领域前沿·中国
从快速抗抑郁的统一机制到精准治疗新策略: 腺苷信号通路的发现与展望
乐晨雨 罗敏敏*
(北京脑科学与类脑研究所; 中国医学科学院北京脑研究所, 北京协和医学院, 北京 102200)
| 罗敏敏, 1973年出生, 神经生物学家, 博士生导师, 特聘研究员。毕业于北京大学和宾夕法尼亚大学。现为北京脑科学与类脑研究所所长、新基石研究员。罗敏敏长期深耕奖惩处理的神经基础理论、神经科学新技术及脑重大疾病新疗法。主要贡献涵盖理论与技术两大领域: 理论上, 提出了5-羟色胺及多巴胺奖赏双轨理论, 并揭示了腺苷在快速抗抑郁疗法中的核心功能; 技术上, 领衔发明了被广泛使用的光纤记录系统、多种脑疾病基因疗法, 以及全球领先的无线高通量侵入式脑机接口系统。 |
从快速抗抑郁的统一机制到精准治疗新策略: 腺苷信号通路的发现与展望
乐晨雨 罗敏敏*
(北京脑科学与类脑研究所; 中国医学科学院北京脑研究所, 北京协和医学院, 北京 102200)
【摘要】抑郁症是全球主要的精神健康挑战之一, 传统抗抑郁药物起效缓慢且治疗率有限。以氯胺酮(Ketamine)和电休克疗法(ECT)为代表的快速抗抑郁干预手段为难治性抑郁症患者带来了希望, 但其背后的神经生物学机制长期以来是领域内的核心谜题。传统理论认为氯胺酮主要通过阻断NMDA受体(NMDAR)发挥作用, 然而这一假说无法完全解释其复杂的生物学效应, 基于该靶点的新药研发也屡屡受挫。该文以近期在Nature发表的研究为核心, 系统性地回顾了探寻快速抗抑郁统一机制的科学历程。该研究首次证实, 无论是药理学的氯胺酮还是物理干预的ECT, 其快速抗抑郁效应均由一个共同的下游通路—大脑内侧前额叶皮层(mPFC)的腺苷(adenosine)信号通路驱动[1]。该文将深入阐述这一发现的关键实验证据, 并提出一个全新的概念框架: 氯胺酮作为一种“代谢性神经调控剂”(metabolic neuromodulator), 通过直接作用于线粒体, 引发可控的细胞能量代谢扰动, 该代谢信号被腺苷系统“放大”并转化为强大的神经调控和抗抑郁效应。基于此, 该文还将探讨如何利用这一新机制指导表型药物发现(phenotypic drug discovery)和开发非药物干预新策略(如急性间歇性低氧), 从而实现疗效与副作用的分离。最后, 该文将展望以“代谢–神经轴”(metabolicneural axis)为核心的抑郁症精准治疗的未来, 包括生物标志物开发、个体化神经调控以及整合治疗新范式。
【关键词】抑郁症; 快速抗抑郁; 氯胺酮; 腺苷; 能量代谢; 线粒体; 代谢性神经调控剂; 表型药物发现
The Adenosine Pathway: a Unified Mechanism for Rapid Antidepressant Action and Precision Therapy
YUE Chenyu, LUO Minmin*
(Chinese Institute for Brain Research (Beijing); Beijing Institute for Brain Research, Chinese Academy of Medical Sciences and Peking Union Medical College, Beijing 102200, China)
【Abstract】MDD (major depressive disorder) remains a major global health challenge, with conventional antidepressants often exhibiting delayed onset and limited efficacy. Rapid-acting interventions like ketamine and ECT (electroconvulsive therapy) offer promise, yet their underlying mechanisms have been unclear. The traditional hypothesis holds that ketamine acts primarily by blocking NMDA (N-methyl-D-aspartate) receptors; however, this view cannot fully explain its complex biological effects, and drug development based on this target has repeatedly encountered setbacks. Centered on a recent study published in Nature, this article systematically reviews the scientific journey toward identifying a unified mechanism for rapid antidepressant action. This work demonstrates for the first time that the rapid antidepressant effects of both pharmacological (ketamine) and physical (ECT) interventions are driven by a common downstream pathway—the adenosine signaling pathway in the mPFC (medial prefrontal cortex). This article elaborats on the key experimental evidence supporting this discovery and proposes a novel conceptual framework: ketamine acts as a “metabolic neuromodulator” that directly targets mitochondria, triggering a controlled perturbation of cellular energy metabolism. This metabolic signal is then “amplified” by the adenosine system and translated into potent neural modulation and antidepressant effects. Building on this mechanism, this article further discusses how this new understanding can guide phenotypic drug discovery and the development of non‑pharmacological intervention strategies (such as acute intermittent hypoxia) to dissociate therapeutic effects from side effects. Finally, this article offers a perspective on a future of precision MDD treatment centered on the“metabolic‑neural axis”, including the development of biomarkers, individualized neuromodulation, and integrated therapeutic paradigms.
【Keywords】MDD; rapid antidepressant; ketamine; adenosine; energy metabolism; mitochondria; metabolic neuromodulator; phenotypic drug discovery
抑郁症(major depressive disorder, MDD)已成为困扰全球数亿人的“情绪流感”, 其病理机制复杂, 涉及遗传、环境、神经生化等多重因素[1-3]。尽管以选
择性5-羟色胺再摄取抑制剂(selective serotonin reuptake inhibitors, SSRIs)为代表的传统抗抑郁药物在临床上得到广泛应用, 但它们普遍存在起效缓慢(通常
需要数周)、有效率不高(约三分之一患者无效)以及副作用显著等局限性[4], 对于具有严重自杀倾向的重度抑郁症患者更是远水难解近渴。
21世纪初, 氯胺酮(ketamine)[一种经典的NMDA(N-methyl-D-aspartate)受体非竞争性拮抗剂]在低剂量下能够于数小时内产生快速、强效且持久的抗抑郁效果的发现, 被认为是精神药理学领域近半个世纪以来最重要的突破之一[5-7]。这一发现不仅为大量难治性抑郁症患者带来了曙光, 也彻底改变了学界对抑郁症病理生理和药物研发的认知。几乎在同一时期, 拥有悠久历史的物理干预手段—电休克疗法(electroconvulsive therapy, ECT)的快速抗抑郁效应也再次受到重视。氯胺酮与ECT, 一个是小分子药物, 一个是物理能量刺激, 作用方式迥异, 却共同指向了一个激动人心的可能性: 大脑中或许存在一个能够被快速激活从而迅速逆转抑郁状态的“总开关”。
然而, 这个“总开关”究竟是什么?传统的“NMDAR(N-methyl-D-aspartate receptor)假说”虽然为氯胺酮的研究提供了起点, 但随着研究深入, 其局限性日益凸显: 氯胺酮的代谢产物在几乎不作用于NMDAR的情况下依然具有抗抑郁活性[8]; 更重要的是, 多家国际制药公司投入巨资开发的、选择性更高的NMDAR拮抗剂, 在临床试验中相继失败[9-10]。这表明, NMDAR阻断或许只是故事的开端, 而非全部。该领域迫切需要一个新的、更具解释力的统一理论框架, 来阐明这些不同疗法背后共同的生物学靶点。
本综述将以我们团队近期的研究为主线, 系统性地阐述我们如何从这个困扰神经科学界十余年的难题出发, 通过一系列环环相扣的实验, 最终锁定腺苷信号通路作为驱动快速抗抑郁效应的核心枢纽,并在此基础上提出新的理论、开发新的疗法[11]。
1 腺苷: 从能量代谢物到关键神经调控分子的“双重身份”
腺苷(adenosine)是生命体中最基本、最古老的分子之一。在细胞生物学的经典教科书中, 它以三磷酸腺苷(ATP)核心组分的形式广为人知, 是细胞进行一切生命活动的“能量货币”。然而, 在神经科学领域, 腺苷还扮演着另一个至关重要的角色—一个强大的神经调控分子(neuromodulator)。当神经元活动剧烈、能量消耗增加时, 细胞内外的腺苷水平就会相应升高。这个升高的腺苷信号, 如同一位尽职的“监督员”, 通过作用于细胞表面的特定受体, 向神经系统发出“减速”和“保护”的指令[12]。
腺苷的信号功能主要通过四种G蛋白偶联受体(G protein-coupled receptors, GPCRs)来实现, 即A1、A2A、A2B和A3受体。这四种受体在大脑中分布广泛但各有侧重, 介导的功能也十分多样。其中, A1受体与抑制性的Gi/o蛋白偶联, 其激活通常会抑制神经元放电、减少神经递质释放, 发挥着“踩刹车”的作用, 是大脑内主要的抑制性调控系统之一。相反, A2A受体主要与兴奋性的Gs蛋白偶联, 其激活则倾向于增强突触传递和可塑性, 扮演着“踩油门”的角色。A1和A2A受体对腺苷的亲和力最高, 因此被认为是腺苷在生理浓度下发挥神经调控作用的主要介导者[12-14]。
正是凭借这种调节神经元兴奋性和突触功能的能力, 腺苷系统深度参与了对多种高级脑功能的调控, 包括睡眠–觉醒周期、学习记忆、动机和情绪等[12-13,15]。例如, 我们在日常生活中感受到的睡意,很大程度上就是由大脑中腺苷在清醒期间不断累积所驱动的; 而咖啡因能提神的主要机制, 是通过阻断腺苷受体, 直接削弱腺苷对神经活动的抑制, 从而驱散睡意[16-18]。
近年来, 越来越多的证据表明, 腺苷系统功能的失调与抑郁症的病理生理密切相关[15,19]。一些临床前研究发现, 增强A1受体信号或抑制A2A受体信号, 通常能产生抗抑郁样的行为效应[20-21]。此外, 一些已知的、能增强内源性腺苷信号的干预手段, 如睡眠剥夺和生酮饮食, 也均被证实具有快速的抗抑郁效果[22-24]。这些线索共同指向了一个充满吸引力的可能性: 调控腺苷信号通路, 或许是实现快速抗抑郁的一条潜藏的关键路径。然而, 在我们的研究之前, 尚无直接证据将这一通路与氯胺酮、ECT等临床上最有效的快速抗抑郁疗法联系起来。
2 统一通路的发现: 腺苷信号是核心枢纽
我们研究的核心起点是提出一个大胆的假设:如果氯胺酮和ECT存在共同机制, 那么它们应该在大脑中引起相似的分子或信号变化。利用我们与合作者开发的基因编码的腺苷荧光探针(GRABado)[25], 结合光纤记录技术, 我们首次得以在清醒活动的小鼠大脑中实时、高灵敏度地“看到”腺苷分子的动态变化。
2.1 氯胺酮与ECT共同诱导mPFC腺苷水平的快速、持续性升高
实验结果令人振奋: 无论是注射低剂量氯胺酮,还是施加单次ECT刺激, 我们都在与情绪和高级认知功能密切相关的关键脑区—内侧前额叶皮层[mPFC(medial prefrontal cortex)]—观测到了腺苷水平快速、大幅度且持续性的升高(图1A)。这一现象在抑郁模型小鼠和正常小鼠中均能稳定复现, 提示腺苷信号的激活是这些疗法一个极具共性的、基础的生物学效应。
2.2 腺苷信号通路介导抗抑郁效应的因果关系验证
相关性不等于因果性。为了证明腺苷信号升高是“原因”而非“结果”, 我们进行了经典的“阻断”(loss-of-function)和“模拟”(gain-of-function)实验。我们利用基因敲除小鼠, 特异性地去除了大脑中接收腺苷信号的两个关键受体—A1和A2A受体。结果发现, 在这些敲除小鼠中, 氯胺酮和ECT的抗抑郁效果完全消失。反之, 如果我们绕过氯胺酮, 直接向抑郁模型小鼠大脑中注射腺苷, 或用光遗传学技术精准激活mPFC脑区的星形胶质细胞以促进内源性腺苷释放, 均能完美地模拟出快速抗抑郁效应(图1B)。这一系列的证据共同确立了腺苷信号通路在介导快速抗抑郁效应中的核心与必要地位。
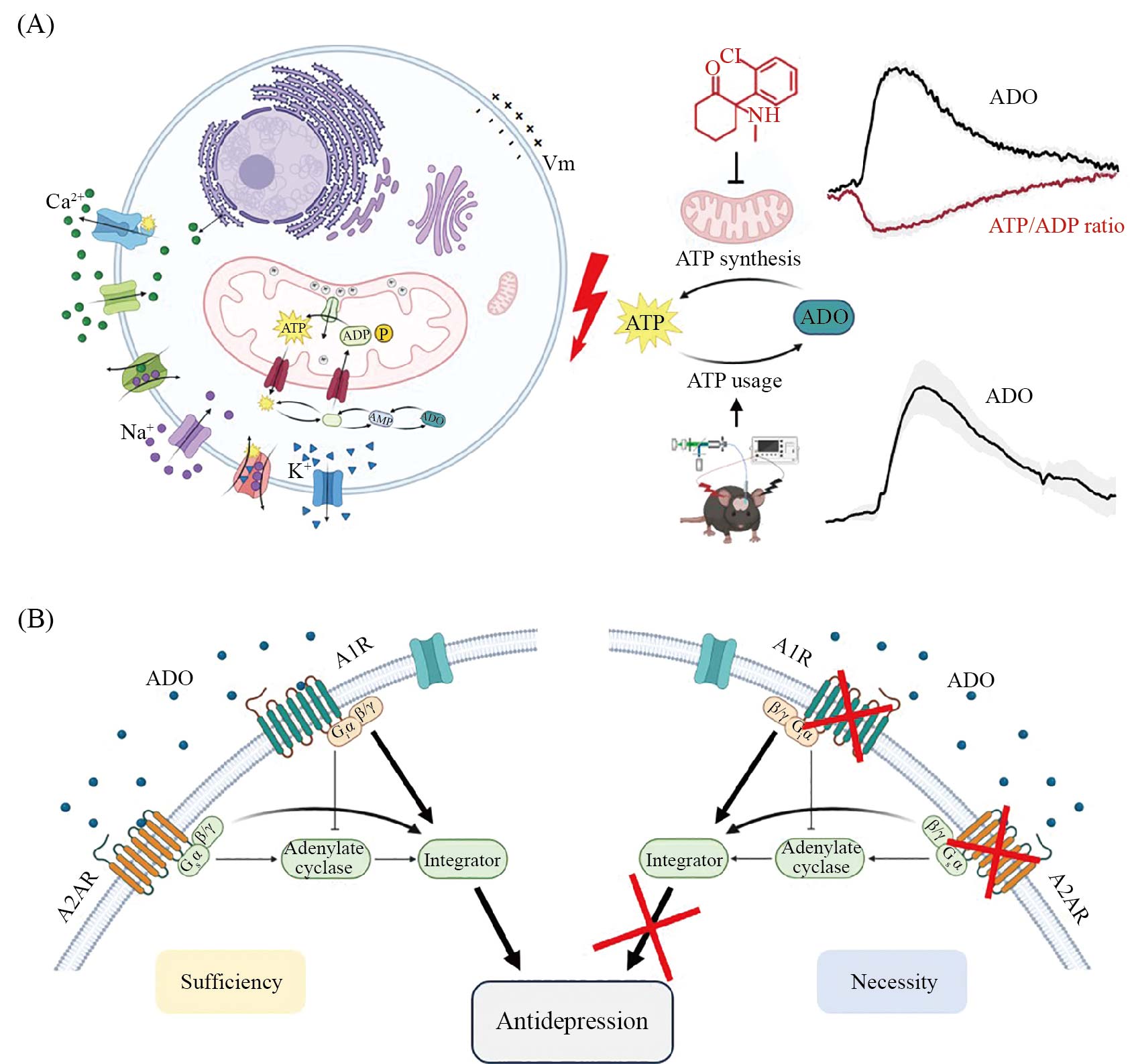
A: 两种快速抗抑郁干预手段, 药理学的氯胺酮(ketamine)和物理干预的电休克疗法(ECT), 尽管上游作用方式不同, 但均能诱导大脑内侧前额叶皮层(mPFC)细胞外腺苷(adenosine, ADO)水平的快速、持续性升高。B: 释放的腺苷作用于神经元上的A1和A2A受体, 激活下游信号通路, 从而产生快速抗抑郁的治疗效果。通过遗传学(A1R/A2AR KO)或药理学手段阻断腺苷受体, 则氯胺酮与ECT的抗抑郁效应被消除; 反之, 直接激活腺苷信号通路(注射腺苷或光遗传学刺激), 则可模拟出抗抑郁效应。
A: two rapid antidepressant interventions, the pharmacological agent ketamine and the physical intervention ECT (electroconvulsive therapy), though acting through distinct upstream pathways, both induce a rapid and sustained increase in extracellular adenosine levels in the mPFC (medial prefrontal cortex). B: the released adenosine acts on neuronal A1 and A2A receptors, activating downstream signaling pathways to produce rapid antidepressant effects. Blocking adenosine receptors via genetic (A1R/A2AR KO) or pharmacological means abolishes the antidepressant effects of both ketamine and ECT; conversely, directly activating the adenosine pathway (adenosine injection or optogenetic stimulation) can mimic the antidepressant effect.
图1 腺苷信号通路作为快速抗抑郁疗法共同机制的示意模型(使用BioRender绘制)
Fig.1 Schematic model illustrating the adenosine signaling pathway as a common mechanism underlying rapid antidepressant therapies (made by BioRender)
3 新机制的提出: 氯胺酮是一种代谢性神经调控剂
既然确定了腺苷是核心分子, 一个更深层次的问题随之而来: 氯胺酮是如何让大脑释放腺苷的?传统的腺苷释放理论主要指向细胞损伤时ATP的大量外流并水解, 但这显然无法解释低剂量氯胺酮在无神经毒性情况下产生的治疗效应。
3.1 腺苷释放源于细胞内能量代谢的改变
通过一系列精巧的实验, 我们排除了“氯胺酮通过诱导细胞外ATP水解来增加胞外腺苷”这一假设。进一步的研究发现, 氯胺酮能够直接作用于细胞的能量工厂—线粒体, 在治疗相关浓度下, 显著抑制线粒体三羧酸循环(tricarboxylic acid cycle, TCA)的代谢流量。这会导致细胞内ATP与ADP的比值(ATP/ADP ratio)迅速下降。细胞内的ATP/ADP值是衡量细胞“能量状态”的关键指标, 它的下降是一个强烈的信号, 促使细胞将多余的腺苷通过平衡性核苷转运体(equilibrative nucleoside transporters, ENTs)“泵”出细胞外(图2)。
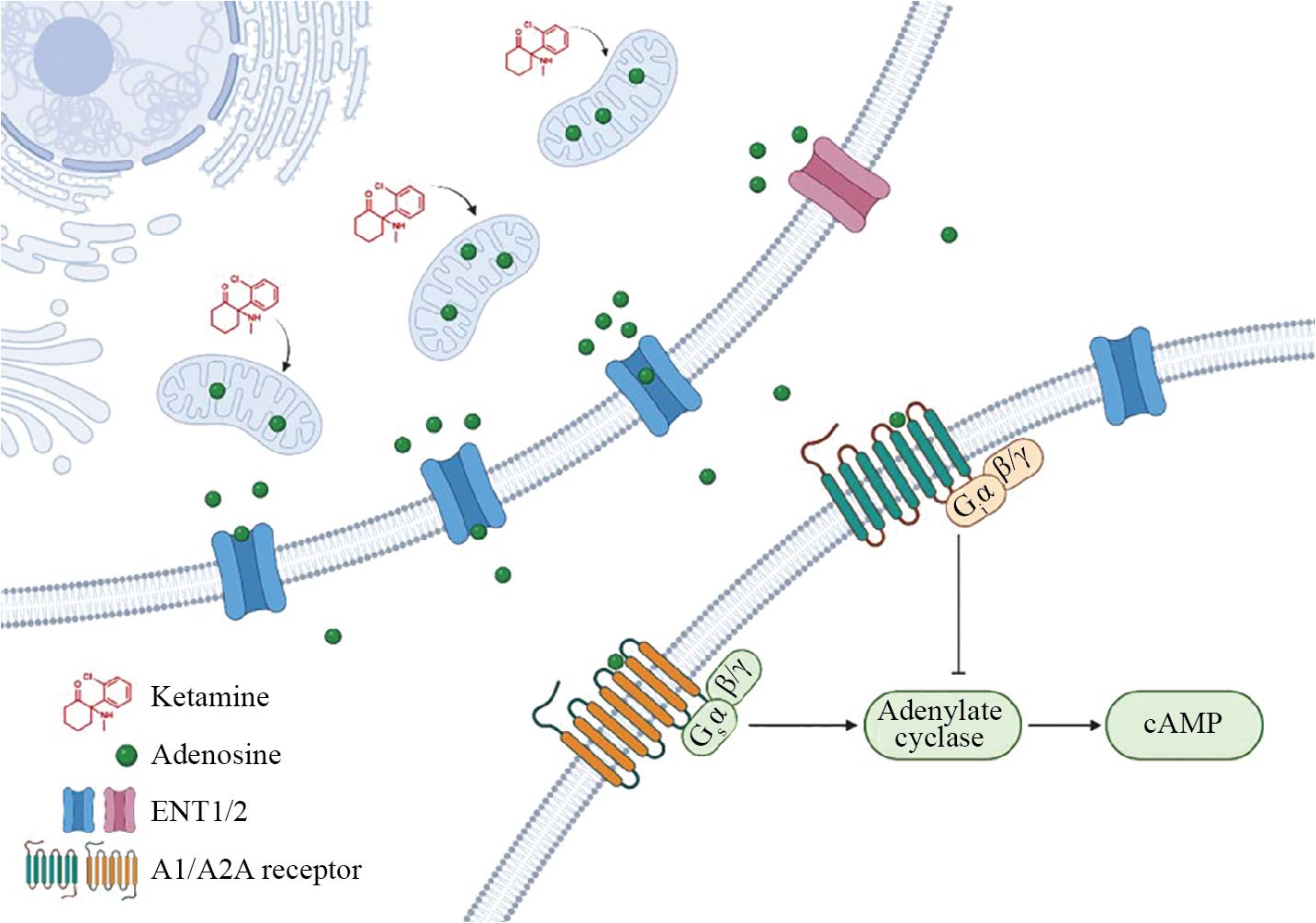
机制模式图: 氯胺酮直接进入细胞并作用于线粒体, 抑制TCA循环, 导致细胞内ATP/ADP值下降。这一代谢信号促使腺苷通过ENTs释放至细胞外。由于胞内外浓度差异显著, 微小的代谢变化被放大为强烈的腺苷信号。
Schematic diagram of the mechanism: ketamine directly enters cells and acts on mitochondria, inhibiting the TCA cycle and leading to a decrease in the intracellular ATP/ADP ratio. This metabolic signal promotes adenosine release into the extracellular space via ENTs (equilibrative nucleoside transporters). Due to the vast concentration gradient between intracellular and extracellular compartments, subtle metabolic changes are amplified into a significant adenosine signal.
图2 氯胺酮作为“代谢性神经调控剂”的作用机制(使用BioRender绘制)
Fig.2 Mechanism of ketamine as a “metabolic neuromodulator” (made by BioRender)
3.2 代谢信号的放大: 从ATP到腺苷的“杠杆效应”
这一机制的精妙之处在于一个“信号放大”原理。细胞内的ATP浓度高达毫摩尔(mmol/L)级别, 而细胞外的腺苷浓度则在纳摩尔(nmol/L)级别, 两者相差成千上万倍。这意味着, 一个由氯胺酮引起的、对ATP总量来说微不足道的代谢扰动, 就足以被“杠杆式”地放大为细胞外腺苷信号的剧烈变化。这完美地解释了为何低剂量氯胺酮能产生如此强大的神经调控作用。
基于此, 我们提出了一个全新的概念框架: 氯胺酮本质上是一种“代谢性神经调控剂”。它的抗抑郁作用并非始于细胞表面的离子通道, 而是始于细胞内部的线粒体。它通过施加一个短暂、可控的“代谢挑战”(metabolic challenge), “劫持”细胞最基本的能量稳态调节通路, 并将其转化为一个强有力的抗抑郁神经信号。
4 从机制到应用: 新一代疗法的蓝图
一个好的科学发现, 其价值最终体现在能否指导实践、解决问题。腺苷通路这一新机制为开发更安全、更有效的抗抑郁疗法提供了清晰的路线图。
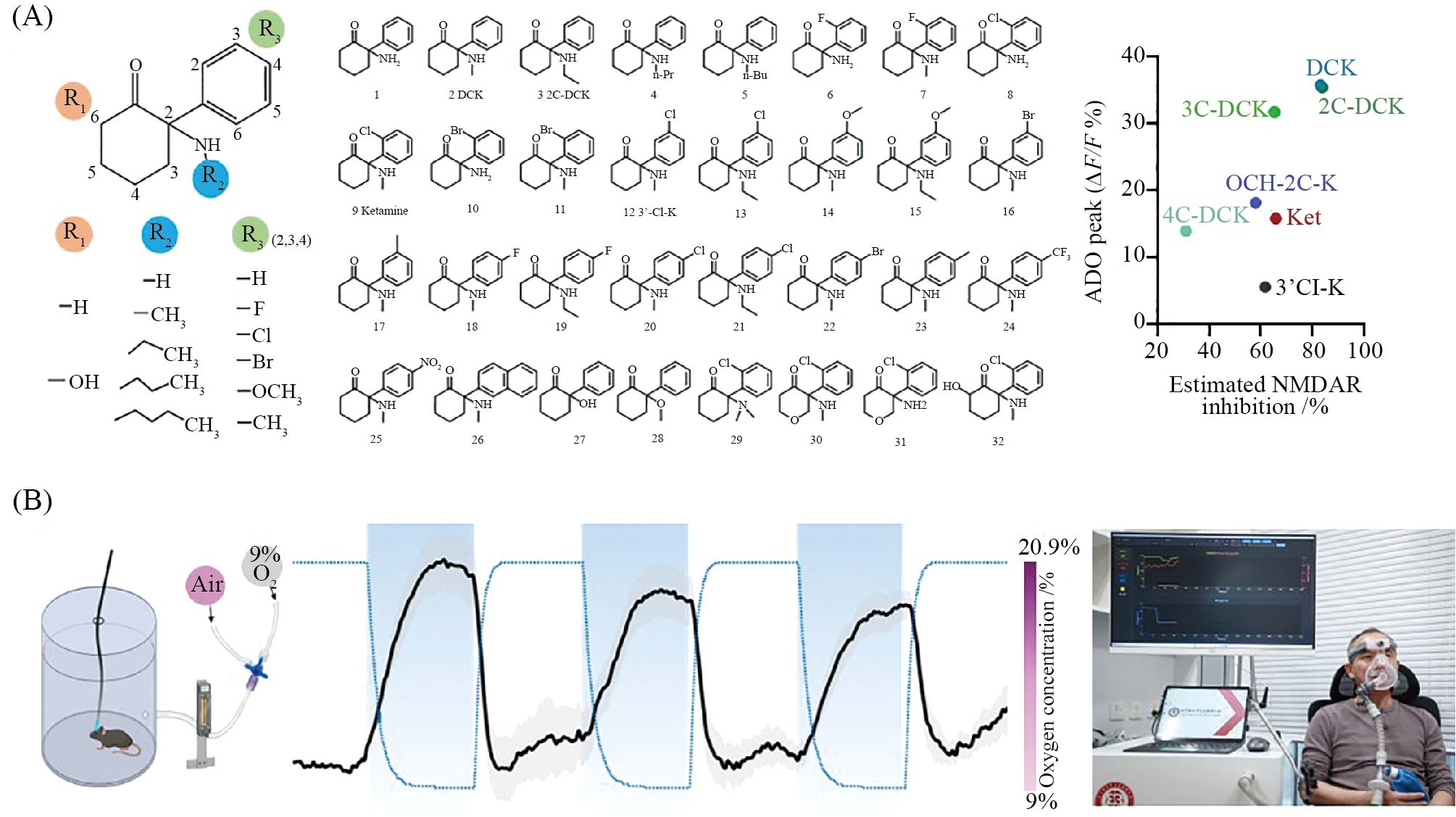
A: 基于新机制的表型药物筛选, 散点图展示了不同氯胺酮衍生物的腺苷释放效能(纵轴)与其对NMDA受体的抑制强度(横轴)之间的关系。可见,以DCK为代表的新分子, 其强大的腺苷释放能力与NMDAR抑制强度并无直接关联, 这一结果验证了新机制的独立性, 并指导了新药发现。B:基于新机制的非药物疗法的开发, 图中展示了急性间歇性低氧(aIH)能够快速调控大脑腺苷变化, 以及开发出可用于临床的低氧设备。
A: phenotype-based drug screening guided by the new mechanism: the scatter plot illustrates the relationship between adenosine release efficacy (vertical axis) and NMDAR inhibition strength (horizontal axis) for different ketamine analogs. Molecules such as DCK demonstrate strong adenosine-releasing capacity largely independent of NMDAR blockade, which supporting the novel mechanism and informing drug discovery. B: development of non-pharmacological interventions based on the new mechanism: the figure illustrates how aIH (acute intermittent hypoxia) rapidly modulates brain adenosine levels and presents a prototype of a hypoxic device developed for potential clinical application.
图3 基于腺苷机制的表型药物筛选和非药物疗法的开发(本图数据点为示意, 改编自参考文献[11])
Fig.3 Development of phenotype-based drug screening and non-pharmacological therapies targeting the adenosine mechanism (data points are schematic, adapted from reference [11])
4.1 表型药物发现: 分离疗效与副作用
传统药物研发遵循“一个靶点、一个药”的模式。但我们既然知道最终的疗效表型是“诱导腺苷释放”, 我们就可以直接以此为筛选指标, 进行“表型药物发现”。我们以此为标准, 合成并筛选了数十种新的氯胺酮衍生物。最终, 我们发现了一种名为去氯氯胺酮(deschloroketamine, DCK)的分子, 它在极低剂量下诱导腺苷释放的能力远超氯胺酮, 并表现出更优的抗抑郁效果。更重要的是, 在同等抗抑郁效果下, 它引起的、与致幻副作用相关的过度活动性显著降低。这从实践上证明, 抗抑郁的疗效通路与副作用通路是可以分离的。
4.2 非药物干预: 急性间歇性低氧(aIH)疗法
既然腺苷释放的本质是应对“能量挑战”, 那么任何能安全模拟这一过程的生理手段, 理论上都应具有抗抑郁潜力。我们由此获得灵感, 开发了一种急性间歇性低氧(acute intermittent hypoxia, aIH)干预方案。通过让抑郁模型小鼠短暂、可控地呼吸低氧空气, 我们成功地在它们大脑中诱导了与氯胺酮类似的腺苷释放, 并产生了依赖于腺苷受体的快速抗抑郁效果。这一发现极具临床转化价值, 因为它为开发一种无创、无化学物质、成本低廉且有望居家使用的抑郁症治疗设备奠定了坚实的生物学基础。
5 研究的潜在意义
本团队的研究系统性地揭示了腺苷信号通路是多种快速抗抑郁疗法背后一个统一的核心机制,并提出了氯胺酮作为“代谢性神经调控剂”的新理论。这一系列发现不仅解答了领域内的长期谜题,更重要的是为抑郁症的未来治疗开辟了全新的方向。
5.1 “代谢–神经轴”作为抑郁症治疗的新靶点
我们的工作将学界的目光从传统的神经递质和受体, 引向了更上游、更基础的细胞能量代谢。以线粒体功能为核心的 “代谢 –神经轴 ”不仅是理解快速抗抑郁机制的关键 , 也可能成为未来抑郁症病理研究和药物开发的一个全新、充满潜力的领域。
5.2 迈向精准精神医学: 生物标志物的开发
未来的关键一步是开发与腺苷通路功能相关的生物标志物(biomarker)。如果我们能通过脑电、血液或功能影像等手段, 无创地评估一个患者大脑的腺苷通路状态, 就有可能在治疗前预测其对相关疗法的反应, 从而实现真正的个体化精准治疗, 改变当前“试错式”的用药模式。
5.3 整合治疗新范式
抑郁症的治疗终将走向整合。我们的发现为整合治疗提供了新的逻辑: 利用快速抗抑郁手段(如新型衍生物或aIH疗法)迅速打开一个宝贵的“治疗窗口期”, 在这个窗口期内, 患者的症状得到缓解, 从而更有能力和意愿配合心理治疗、康复训练, 甚至是更前沿的、针对特定神经环路的精准神经调控[如深部脑刺激(deep brain stimulation, DBS)或基因治疗], 以实现长期的稳定和康复。
总而言之, 腺苷信号通路的发现, 为我们撬动抑郁症这座“冰山”提供了一个新的支点。从基础机制的阐明, 到新药与新疗法的开发, 再到未来精准治疗的蓝图, 我们有理由相信, 在不远的将来, 人类对抗抑郁症的“工具箱”将变得更加丰富、精准和有效。
6 未来研究的关键问题与挑战
腺苷信号通路作为快速抗抑郁核心枢纽的发现, 如同打开了一扇通往新世界的大门, 门内的风景引人入胜, 但同时也充满了更多、更深层次的未知。解答以下几个关键科学问题, 将是未来十年推动该领域实现颠覆性突破的核心挑战。
6.1 上游机制: 氯胺酮的线粒体靶点与代谢调控的分子细节是什么?
尽管我们首次证实了氯胺酮能够直接作用于线粒体并抑制TCA循环, 但这仅仅是故事的开端, 亟待解决的迫切且直接的是以下几个问题。氯胺酮在线粒体内直接结合的分子靶点究竟是什么?这个靶点可能是一种酶、一个转运蛋白, 还是线粒体内膜上的某个复合物, 鉴定出这个精确的分子靶点, 将是实现“源头创新”的关键。一方面, 这将使我们能够设计选择性更高、活性更强的分子化合物。摆脱氯胺酮分子骨架的限制, 基于新靶点的三维结构, 从头设计出专一性作用于线粒体该靶点的小分子激动剂或抑制剂。这类新药有望彻底消除氯胺酮因作用于NMDA受体等“脱靶”靶点而带来的副作用, 实现药效与安全性的最大化。另一方面, 这将使我们能够厘清NMDA受体的确切角色。虽然我们的数据表明, NMDAR抑制与腺苷释放并无直接的线性关系,但它是否扮演了某种“许可”(permissive)或协同的角色?例如, NMDAR的适度抑制是否为线粒体的代谢重编程创造了有利的细胞内环境?通过将靶向线粒体新靶点的药物, 与NMDAR拮抗剂进行组合或比较研究, 将最终厘清这一长期存在的争议。
6.2 下游效应: 腺苷如何重塑神经环路与突触可塑性?
我们的研究在宏观层面连接了“腺苷释放”与“抗抑郁行为”, 但其间的微观桥梁—腺苷如何具体影响神经元活性、重塑神经环路功能, 并最终促进神经可塑性—仍有待深入探索。未来的研究需要回答以下几个问题。(1) 腺苷如何调控神经元放电模式与环路动态?腺苷通过A1受体抑制神经元放电, 通过A2A受体则可能增强突触传递。这两种看似拮抗的作用在一个统一的抗抑郁效应中是如何时空协同、动态平衡的?尤其是在mPFC这个复杂的脑区, 腺苷是如何精准调控兴奋性锥体神经元与多种抑制性中间神经元之间的平衡, 从而“纠正”抑郁状态下失调的环路活动的? (2) 是否存在长期的转录和表观遗传学效应?快速抗抑郁效应的持久性提示,腺苷信号的激活可能不仅仅是短暂地改变神经元兴奋性, 更有可能启动了一系列长期的、涉及基因表达和染色质修饰的程序。例如, 腺苷信号通路是
否是上游信号, 是否通过激活cAMP-PKA-CREB等经典通路, 最终调控如脑源性神经营养因子(brainderived neurotrophic factor, BDNF)等关键可塑性相关分子的表达?探索其背后的转录组与表观遗传学图谱, 将为理解抗抑郁效应如何从“快速启动”走向“长期维持”提供分子基础。
6.3 环路解析: 哪些细胞类型和神经通路是关键执行者?
虽然我们锁定了mPFC是关键脑区, 但mPFC内部是一个异质性极高的复杂结构。未来的环路解析工作需要达到更高的精度。(1) mPFC内的细胞类型特异性贡献是什么? mPFC的不同亚区(如PrL、IL、ACC)、不同投射类型(如投射到杏仁核、伏隔核或丘脑的锥体神经元)以及不同类型的抑制性中间神经元, 在腺苷介导的抗抑郁效应中分别扮演什么角色?利用单细胞测序、病毒工具和在体多通道记录等前沿技术, 绘制一张精细的“腺苷作用环路地图”至关重要。(2) 海马及其他脑区的协同作用是什么?我们的数据显示, 氯胺酮也能诱导海马区的腺苷释放。海马在学习记忆和情绪调节中扮演关键角色,它与mPFC之间存在紧密的结构和功能连接。那么,mPFC和海马区的腺苷信号是如何协同作用的?是否存在一个以“mPFC-海马”连接为核心的、由腺苷调控的抗抑郁关键环路?
6.4 临床转化: 如何监控腺苷信号并解释临床异质性?
要将基础研究的发现真正转化为能惠及广大患者的临床实践, 我们必须跨越从动物模型到人体的鸿沟, 解决临床应用中的实际问题。(1) 如何在人体中无创地监控腺苷信号?这是实现精准治疗的前提。直接测量大脑中的腺苷水平在人体中难以实现。因此, 开发可靠的外周生物标志物迫在眉睫。这个标志物可能是一种与大脑腺苷代谢状态相关的血液代谢物、一种可被脑电图(electroencephalograph,EEG)捕捉到的特定脑电振荡模式(如与A1受体功能相关的慢波活动), 或是一种可被功能性磁共振成像(functional magnetic resonance imaging, fMRI)检测到的特定脑区连接模式。(2) 腺苷通路的功能差异能否解释临床异质性?这是一个极其重要的临床问题:为什么有些患者对氯胺酮或ECT反应良好, 而另一些则无效?我们推测, 这种治疗反应的异质性, 很可能源于患者个体间腺苷通路本身的功能差异。例如,某些患者可能存在腺苷合成、释放、转运或受体功能相关的基因多态性或功能缺陷。未来, 通过结合基因组学、影像学和临床队列研究, 验证“腺苷通路功能假说”, 将为实现患者分层、疗效预测以及为无效患者开发替代或增效策略提供坚实的科学依据。
参考文献 (References)
[1] OTTE C, GOLD S M, PENNINX B W, et al. Major depressive disorder [J]. Nat Rev Dis Primers, 2016, 2: 16065.
[2] CUI L, LI S, WANG S, et al. Major depressive disorder: hypothesis, mechanism, prevention and treatment [J]. Signal Transduct Target Ther, 2024, 9(1): 30.
[3] FRIES G R, SALDANA V A, FINNSTEIN J, et al. Molecular pathways of major depressive disorder converge on the synapse [J]. Mol Psychiatry, 2023, 28(1): 284-97.
[4] ABDALLAH C G, SANACORA G, DUMAN R S, et al. Ketamine and rapid-acting antidepressants: a window into a new
neurobiology for mood disorder therapeutics [J]. Annu Rev Med, 2015, 66: 509-23.
[5] BERMAN R M, CAPPIELLO A, ANAND A, et al. Antidepressant effects of ketamine in depressed patients [J]. Biol Psychiatry, 2000, 47(4): 351-4.
[6] ZARATE C A, JR, SINGH J B, CARLSON P J, et al. A randomized trial of an N-methyl-D-aspartate antagonist in treatmentresistant major depression [J]. Arch Gen Psychiatry, 2006, 63(8): 856-64.
[7] KRYSTAL J H, ABDALLAH C G, SANACORA G, et al. Ketamine: a paradigm shift for depression research and treatment [J]. Neuron, 2019, 101(5): 774-8.
[8] ZANOS P, MOADDEL R, MORRIS P J, et al. NMDAR inhibition- independent antidepressant actions of ketamine metabolites [J]. Nature, 2016, 533(7604): 481-6.
[9] KIM J W, SUZUKI K, KAVALALI E T, et al. Ketamine: mechanisms and relevance to treatment of depression [J]. Annu Rev Med, 2024, 75: 129-43.
[10] HILLHOUSE T M, PORTER J H. A brief history of the development of antidepressant drugs: from monoamines to glutamate [J]. Exp Clin Psychopharmacol, 2015, 23(1): 1-21.
[11] YUE C, WANG N, ZHAI H, et al. Adenosine signalling drives antidepressant actions of ketamine and ECT [J]. Nature, 2026, 649(8096): 423-31.
[12] DUNWIDDIE T V, MASINO S A. The role and regulation of adenosine in the central nervous system [J]. Annu Rev Neurosci, 2001, 24: 31-55.
[13] BOREA P A, GESSI S, MERIGHI S, et al. Pharmacology of adenosine receptors: the state of the art [J]. Physiol Rev, 2018, 98(3): 1591-625.
[14] VINCENZI F, PASQUINI S, CONTRI C, et al. Pharmacology of adenosine receptors: recent advancements [J]. Biomolecules, 2023, 13(9): 1387.
[15] VAN CALKER D, BIBER K, DOMSCHKE K, et al. The role of adenosine receptors in mood and anxiety disorders [J]. J Neurochem, 2019, 151(1): 11-27.
[16] PENG W, WU Z, SONG K, et al. Regulation of sleep homeostasis mediator adenosine by basal forebrain glutamatergic neurons [J]. Science, 2020, 369(6508): eabb0556.
[17] FREDHOLM B B, BATTIG K, HOLMEN J, et al. Actions of caffeine in the brain with special reference to factors that contribute to its widespread use [J]. Pharmacol Rev, 1999, 51(1): 83- 133.
[18] LOPES J P, PLIASSOVA A, CUNHA R A. The physiological effects of caffeine on synaptic transmission and plasticity in the mouse hippocampus selectively depend on adenosine A(1) and A(2A) receptors [J]. Biochem Pharmacol, 2019, 166: 313-21.
[19] SPERLAGH B, CSOLLE C, ANDO R D, et al. The role of purinergic signaling in depressive disorders [J]. Neuropsychopharmacol Hung, 2012, 14(4): 231-8.
[20] SERCHOV T, CLEMENT H W, SCHWARZ M K, et al. Increased signaling via adenosine A1 receptors, sleep deprivation, imipramine, and ketamine inhibit depressive-like behavior via induction of homer1a [J]. Neuron, 2015, 87(3): 549-62.
[21] CUNHA M P, PAZINI F L, ROSA J M, et al. Creatine, similarly to ketamine, affords antidepressant-like effects in the tail suspension
test via adenosine A(1) and A2A receptor activation [J]. Purinergic Signal, 2015, 11(2): 215-27.
[22] HINES D J, SCHMITT L I, HINES R M, et al. Antidepressant effects of sleep deprivation require astrocyte-dependent adenosine mediated signaling [J]. Transl Psychiatry, 2013, 3(1): e212.
[23] RUSKIN D N, KAWAMURA M, MASINO S A. Adenosine and ketogenic treatments [J]. J Caffeine Adenosine Res, 2020, 10(3):
104-9.
[24] MASINO S A, KAWAMURA M, WASSER C D, et al. Adenosine, ketogenic diet and epilepsy: the emerging therapeutic relationship between metabolism and brain activity [J]. Curr Neuropharmacol, 2009, 7(3): 257-68.
[25] WU Z, CUI Y, WANG H, et al. Neuronal activity-induced, equilibrative nucleoside transporter-dependent, somatodendritic adenosine release revealed by a GRAB sensor [J]. Proc Natl Acad Sci USA, 2023, 120(14): e2212387120.




 中文版
中文版 英文版
英文版