领域前沿·中国
H3K14ub驱动的异染色质形成与稳态遗传
黄园勇1,2,3* 齐红云4 陈德桂4 翁杰敏1,2,3*
(1华东师范大学附属芜湖医院/芜湖市第二人民医院, 芜湖 241000; 2华东师范大学生命科学学院, 上海市调控生物学重点实验室, 上海 200241; 3上海市奉贤区中心医院, 转化医学联合中心, 上海 201499; 4中国科学院分子细胞科学卓越创新中心/生物化学与细胞生物学研究所, 上海市分子男科学重点实验室, 上海 200031)
| 翁杰敏教授1984年毕业于武汉大学生物系, 1987年获得中国科学院上海细胞生物学研究所硕士学位, 1994年获得美国University of Vermont博士学位, 1994至1997年在美国国立卫生研究院儿童健康与发育研究所从事博士后研究工作,1997年夏加入Baylor医学院的细胞与分子生物学系建立独立实验室, 并于2003年获得tenured副教授, 2007年底加入华东师范大学生命科学学院, 任特聘教授。2014至2020年任华东师范大学生命科学学院副院长, 2020至2025年6月担任生命科学学院院长。翁杰敏教授长期从事表观遗传调控研究, 在DNA甲基化修饰、组蛋白修饰调控机制与功能、肿瘤表观修饰调控等方面取得了系列创新性成果, 已在国内外核心期刊, 包括Cell、Nature、Science、Mol Cel、Cell Res、Nat Commun、NAR和EMBO J等重要国际学术刊物发表论文150余篇, 文章引用超20 000次, 2014至2025年连续入选高被引中国学者榜单。目前主要学术兼职有中国细胞生物学学会理事、中国细胞生物学学会染色质生物学分会主任等。 |
H3K14ub驱动的异染色质形成与稳态遗传
黄园勇1,2,3* 齐红云4 陈德桂4 翁杰敏1,2,3*
(1华东师范大学附属芜湖医院/芜湖市第二人民医院, 芜湖 241000; 2华东师范大学生命科学学院, 上海市调控生物学重点实验室, 上海 200241; 3上海市奉贤区中心医院, 转化医学联合中心, 上海 201499; 4中国科学院分子细胞科学卓越创新中心/生物化学与细胞生物学研究所, 上海市分子男科学重点实验室, 上海 200031)
【摘要】真核生物细胞在有丝分裂过程中需要维持正常且稳定的基因组异染色质与常染色质分区。研究表明异染色质的正确形成、维持和稳态遗传对着丝粒形成、姐妹染色体凝聚与分离、基因组稳定性及基因转录调控都具有重要的生物学意义, 其不稳定性会增加癌症、衰老、神经退行性疾病等疾病风险。长期以来, 甲基转移酶SUV39H介导的H3K9甲基化自模板“读写”机制被认为是细胞分裂过程中异染色质重新组装形成、维持和稳态遗传的核心机制。该研究发现哺乳动物细胞SUV39H的H3K9甲基化的自我读写能力不足以在有丝分裂过程中实现近着丝粒异染色质的稳态传承, 还需要H3K14的泛素化的帮助。具体来说, 研究团队通过筛选鉴定发现泛素连接酶G2E3能够特异催化组蛋白H3K14位点的单泛素化修饰(H3K14ub), 并且G2E3特异定位于近着丝粒异染色质且特异性催化近着丝粒异染色质区域H3K14ub。重要的是, 该研究发现在细胞分裂过程中G2E3催化的H3K14ub是SUV39H近着丝粒异染色定位和催化H3K9me3修饰所必需的。在分子机制上, G2E3在G2/M期高表达, 并以RNA依赖的方式结合有丝分裂染色体的近着丝粒异染色质,通过其催化的H3K14ub修饰, 招募SUV39H, 促进H3K9me3修饰和后续异染色质蛋白HP1的结合与扩散, 从而实现异染色质重新组装形成和稳态遗传。研究还揭示H3K14ub招募SUV39H是通过SUV39H的Chromo结构域, 发现该结构域不仅识别H3K9甲基化, 还识别H3K14ub, 且主要依赖结合H3K14ub而靶向近着丝粒异染色质。此外, G2E3缺失不仅严重损害了近着丝粒异染色质组装, 还导致了SUV39H和H3K9me3在常染色质区域广泛且异常积累, 基因转录广谱抑制。因此, 该研究揭示了H3K14ub驱动的H3K9me3是近着丝粒异染色质形成、维持和稳态遗传的重要机制, 该机制在进化上保守, 且对细胞分裂过程中基因组异染色质与常染色质的正常分区、基因转录调控至关重要。
【关键词】异染色质; 常染色质; G2E3泛素连接酶; H3K14ub; SUV39H1/2; H3K9me3; 异染色质起始; 异染色质维持
A H3K14ub-Driven Heterochromatin Formation and Stable Inheritance Pathway
HUANG Yuanyong1,2,3*, QI Hongyun4, CHEN Degui4, WONG Jiemin1,2,3*
(1Wuhu Hospital, East China Normal University (the Second People’s Hospital, Wuhu), Wuhu 241000, China; 2Shanghai Key Laboratory of Regulatory Biology, Institute of Biomedical Sciences and School of Life Sciences, East China Normal University, Shanghai 200241, China; 3Joint Center for Translational Medicine, Fengxian District Central Hospital, Shanghai 201499, China; 4Shanghai Key Laboratory of Molecular Andrology, Center for Excellence in Molecular Cell Science, Shanghai Institute of Biochemistry and Cell Biology, Chinese Academy of Sciences, Shanghai 200031, China)
【Abstract】Maintaining proper and stable compartmentalization of eukaryotic genome into heterochromatin and euchromatin during mitosis, along with heterochromatin proper reassembly, maintenance and inheritance, are of critical biological significance for centromere assembly, sister chromatid cohesion and separation, genomic integrity and stability, and transcriptional regulation. Heterochromatin instability increases the risk of cancer, aging and related diseases, neurodegenerative disorders. Previous studies suggest a self-templating pathway involving “readwrite”of H3K9 methylation by methyltransferase SUV39H as the core mechanism for heterochromatin reassembly, maintenance and inheritance during mitosis. This study reveals that the “read-write” of H3K9 methylation by SUV39H in mammalian cells is insufficient to achieve stable inheritance of pericentromeric heterochromatin during mitosis, requiring additional assistance from H3K14 ubiquitination. Researchers identified G2E3 as an H3K14ubspecific, pericentromeric heterochromatin-localized E3 ligase. Importantly, H3K14ub catalyzed by G2E3 during mitosis is essential for SUV39H targeting to pericentromeric heterochromatin and for its methyltransferase activity. Mechanistically, G2E3 is highly expressed during G2/M phase, and RNA-dependently binds to pericentromeric heterochromatin on mitotic chromosomes and catalyzes H3K14ub, which is essential for subsequent sequential SUV39H and HP1 targeting to pericentromeric heterochromatin, facilitating H3K9me3 accumulation and spreading to ensure heterochromatin reassembly and inheritance. Researchers further revealed the chromodomain of SUV39H is a dual reader of H3K14ub and H3K9me3, with H3K14ub binding being primary for pericentromeric localization. Notably, the absence of G2E3 not only severely impairs pericentromeric heterochromatin reassembly but also leads to aberrant accumulation of SUV39H and H3K9me3 in numerous euchromatic regions and a widespread transcriptional repression. Thus, this study reveals H3K14ub-driven H3K9me3 as a conserved mechanism of pericentromeric heterochromatin reassembly, maintenance and inheritance, which is in turn crucial for proper genomic chromatin compartmentalization and transcriptional regulation.
【Keywords】heterochromatin; euchromatin; G2E3 ubiquitin ligase; H3K14ub; SUV39H1/2; H3K9me3; heterochromatin initiation; heterochromatin maintenance
1 异染色质的形成与稳态遗传
真核生物基因组由高度浓缩的转录抑制性的异染色质和分散的具有转录活性的常染色质组成。异染色质又分为组成型异染色质和兼性异染色质,其中组成型异染色质主要存在于基因稀少且含有大量重复序列的着丝粒和近着丝粒区域、反转录转座子元件及端粒[1-3]。异染色质对着丝粒形成、姐妹染色体凝聚与分离、基因组完整性和稳定性及基因转录调控至关重要[4-6]。异染色质不稳定或难以形成会造成一系列严重的细胞学和遗传学后果: 转座子激活, 插入突变, 染色体重排、断裂与丢失; 着丝粒形成和姐妹染色体凝聚与分离异常; 基因表达异常; 癌症、衰老、神经退行性疾病等发生[1,7-9]。
在细胞分裂过程中, 高度浓缩的异染色质会随着DNA复制而经历核小体解聚、重新组装, 并将异染色质特征性表观修饰如H3K9甲基化传递给新组装的核小体, 从而确保异染色质结构与功能的稳态遗传。异染色质重新形成、维持和稳态遗传的调控机制在裂殖酵母至哺乳动物中都高度保守, 且在裂殖酵母中研究最为深入, 涉及到组蛋白修饰与RNA调控[1,10]。
异染色质的重新形成、维持与稳态遗传高度依赖于组蛋白H3的9号赖氨酸(K9)的甲基化修饰[11-13]。在裂殖酵母细胞中异染色质的H3K9二甲基化修饰(H3K-9me2)和哺乳动物细胞中异染色质的H3K9三甲基化修饰(H3K9me3)分别由甲基化酶Clr4和SUV39H1/2催化。H3K9甲基化作为异染色质特异组蛋白修饰,可招募裂殖酵母和哺乳动物的异染色质结合蛋白Swi6和HP1定位于异染色质, 并通过蛋白间相互作用招募H3K9甲基化酶Clr4和SUV39H1/2, 促进异染色质H3K9甲基化[14-17]; 同时, Clr4和SUV39H1/2蛋白本身也含有可与H3K9甲基化直接结合的Chromo结构域, 能够在识别并结合H3K9甲基化而定位到异染色质的同时催化生成新的H3K9甲基化修饰。这种自我“读写”机制被认为是异染色质重新形成、维持和稳态遗传的核心基础[1,18]。此外, 大量研究表明源自近着丝粒重复序列的RNA转录本在裂殖酵母和哺乳动物中均参与甲基转移酶CLRC复合体和SUV39H的招募及异染色质的形成[10,19-24]。
虽然上述的H3K9甲基化酶的自我“读写”机制能很好解释异染色质在有丝分裂过程中的稳态传承问题, 但多年来困扰该理论的一个问题是在裂殖酵母中H3K9甲基化酶Clr4与泛素连接酶Cul4以及支架蛋白形成甲基转移酶复合体CLRC, 并且Cul4的泛素连接酶活性对异染色质重新形成不可或缺[25-27]。最新的研究表明, Cul4具有催化H3K14单泛素化(H3K14ub)的能力, 并能促进Clr4介导的H3K9甲基化[28], 进而促进异染色质重新形成, 但具体机制不明。更关键的问题是, 在哺乳动物细胞中H3K9me3甲基化酶SUV39H1/2以独立形式存在, 并不与Cul4形成复合体, 也没有研究报道哺乳动物的异染色质重新形成与稳态遗传是否与H3K14ub相关。我们研究团队长期专注于表观遗传调控的机制与功能研究, 鉴定并发现了哺乳动物细胞中特异性催化H3K14ub的泛素连接酶G2E3, 揭示了G2E3介导的H3K14ub驱动SUV39H催化H3K9me3, 为近着丝粒异染色质稳态传承所必需。我们的工作还表明H3K14ub驱动的H3K9甲基化是进化上的异染色质形成的保守机制, 不仅是近着丝粒异染色质在有丝分裂过程中稳态遗传的核心机制, 同时还调控基因组染色质的正常区室化。接下来我们将以进化上保守的H3K14ub驱动的H3K9me3修饰在染色质区室化中的作用研究为例[29], 介绍近着丝粒异染色质形成、维持和稳态遗传的调控机制。
2 G2E3特异性催化近着丝粒异染色质H3K14ub修饰
我们的研究相关工起始于合作者中国科学院生物化学与细胞生物学研究所陈德桂研究员团队对小鼠长形精子中泛素化组蛋白的研究。他们通过分离制备泛素化修饰的组蛋白组分偶联质谱鉴定发现, 在小鼠长形精子中存在高峰度的组蛋白H3的K14位点单泛素化修饰(H3K14ub)。对于这个新的组蛋白位点单泛素化修饰当时没有任何相关报道(酵母Cul4具有催化H3K14ub的能力, 并促进Clr4介导的H3K9甲基化的报道于2019年发表[28]), 因此, 他们首先开展了筛选鉴定哺乳动物细胞中催化H3K14ub修饰的泛素连接酶的工作。为了鉴定催化H3K14ub修饰的泛素连接酶, 他们首先合成了模拟H3K14ub的多肽, 通过免疫兔子制备了抗H3K14ub的特异性抗体[29]。随后, 他们构建并筛选了一个包含2 227个氨基酸数大于300的细胞核定位蛋白的cDNA表达文库。其筛选方法是将每个表达质粒分别转染HeLa细胞, 用抗H3K14ub抗体进行免疫荧光染色(IF), 检测H3K14ub信号变化情况。该筛选成功鉴定出两个候选蛋白—G2E3和PHF7, 其过表达显著增强了H3K14ub信号(图1A)。由于PHF7在睾丸组织中特异性表达, 最近有研究报道PHF7在减数分裂后精子细胞中催化H3K14ub修饰[30], 而G2E3在所有组织中均有表达, 因此我们将研究重点聚焦在G2E3及其相关生物学功能。
在HeLa和293T细胞中过表达G2E3, IF和蛋白质免疫印迹(WB)都显示G2E3强烈促进H3K14ub修饰(图1B和图1C)。进一步体外纯化G2E3蛋白和带GST标签的组蛋白H3以及突变体H3K14R, 通过体外泛素化实验证明G2E3是特异性催化H3K14位点单泛素化修饰的泛素连接酶(图1D)。为进一步验证G2E3在细胞中是否特异性催化H3K14ub, 我们分别将FLAG标签的核心组蛋白H2A、H2B、H4、H3以及突变体H3K14R和H3K18R/K23R与Myc标签的G2E3和酶活缺失突变体G2E3m3在293T细胞中共转染, 变性免疫沉淀核心组蛋白, WB结果显示G2E3在细胞中亦特异性催化H3K14ub修饰(图1E)。这些结果表明G2E3是特异性催化H3K14ub的泛素连接酶。
为了探究G2E3对细胞内源H3K14ub修饰的贡献值, 我们在不同细胞中敲低或敲除G2E3, IF或WB检测H3K14ub修饰水平。结果显示G2E3敲低和敲除都导致H3K14ub几乎完全丧失(图1F、图1G和图1I), 表明G2E3是哺乳动物细胞内催化H3K14ub的主要泛素连接酶。同时, 我们观察到细胞内源H3K14ub在细胞核内呈点状分布, 且与小鼠NIH3T3成纤维细胞中DAPI强染色的点状异染色质重合(图1H), 表明H3K14ub定位于近着丝粒异染色质, 当敲除或者敲低G2E3时, 近着丝粒异染色质H3K14ub几乎完全丧失(图1G~图1I)。我们也发现在鼠源和人源细胞中过表达的G2E3都呈点状分布, 且与H3K9me3的点状分布重合, 表明G2E3也定位于近着丝粒异染色质(图1J)。这些数据表明G2E3定位于近着丝粒异染色质, 并特异性催化近着丝粒异染色质H3K14ub修饰。
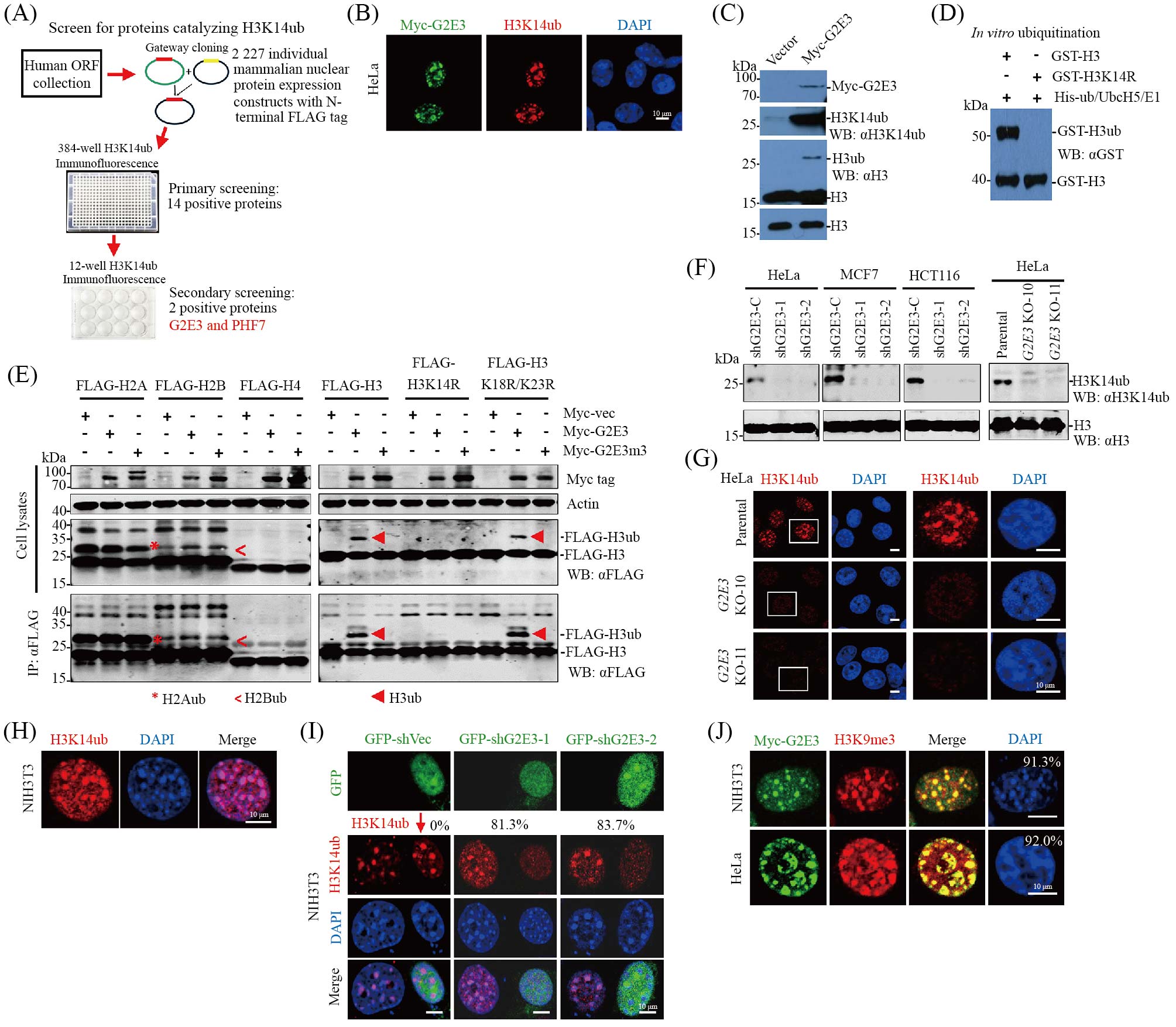
A: H3K14ub的泛素连接酶筛选鉴定示意图。B: HeLa细胞中过表达Myc-G2E3强烈促进H3K14ub修饰。C: 293T细胞中过表达Myc-G2E3强烈促进H3K14ub修饰。D: 体外泛素化实验显示G2E3特异性催化H3K14ub修饰。E: 细胞内过表达G2E3特异性催化H3K14ub修饰。F: 不同细胞中敲低或敲除G2E3导致内源H3K14ub修饰剧烈下降。G: IF显示HeLa细胞内源H3K14ub定位于近着丝粒异染色质, G2E3敲除导致内源H3K14ub修饰剧烈下降。H: IF显示NIH3T3细胞内源H3K14ub定位于近着丝粒异染色质。I: NIH3T3中敲低G2E3导致内源H3K14ub修饰剧烈下降。J: IF显示不同细胞中过表达的G2E3都定位于近着丝粒异染色质。
A: schematic of H3K14ub ubiquitin ligase screening and identification. B: ectopically expressed Myc-G2E3 intensely enhances H3K14ub modification in HeLa cells. C: ectopically expressed Myc-G2E3 intensely enhances H3K14ub modification in 293T cells. D: in vitro ubiquitination assay demonstrates that G2E3 catalyzes H3K14ub specifically. E: ectopically expressed G2E3 catalyzes H3K14ub modification specifically. F: knockdown and knockout G2E3 result in a dramatic decrease of endogenous H3K14ub modification in various cell lines. G: IF shows endogenous H3K14ub localizes on pericentromeric heterochromatin in HeLa cells, and G2E3 knockout causes a dramatic decrease of endogenous H3K14ub modification. H: IF shows endogenous H3K14ub localizes on pericentromeric heterochromatin in NIH3T3 cells. I: knockdown of G2E3 results in a dramatic decrease of endogenous H3K14ub modification in NIH3T3 cells. J: IF shows that ectopically expressed G2E3 localizes on pericentromeric heterochromatin in various cell types.
图1 G2E3定位于近着丝粒异染色质, 特异性催化近着丝粒异染色质H3K14ub修饰(根据参考文献[29]修改)
Fig.1 G2E3 is a pericentromeric heterochromatin associated, H3K14 mono-ubiquitination-specific E3 ligase (modified from reference [29])
3 G2E3酶活依赖性促进SUV39H1/2介导的近着丝粒异染色质H3K9me3修饰
组蛋白修饰之间存在交互调控(cross-talk), 不同修饰之间相互促进或者抑制。之前研究表明组蛋白H2AK119ub与H3K27me3修饰相互促进[31-32], H2BK120ub可促进H3K4me3和H3K79me3修饰[33-34]。因此,我们猜想H3K14ub可能会促进某种组蛋白甲基化修饰, 且鉴于其定位于近着丝粒异染色质, H3K14ub修饰尤其可能促进H3K9甲基化修饰。
在不同细胞中敲低或者敲除G2E3, WB检测各种不同的组蛋白甲基化修饰, 结果显示只有H3K9me3修饰特异性显著降低, 并不影响其他位点的甲基化修饰(图2A)。反过来过表达G2E3时只有H3K9me3修饰特异性上调, 但G2E3酶活缺失突变体并不能促进H3K9me3修饰(图2B~图2D)。此外,无论敲低、敲除或过表达G2E3, 都不会影响催化H3K9me3的关键甲基化酶SUV39H1、SUV39H2和SETDB1的蛋白水平(图2A和图2B), 表明G2E3不是通过影响SUV39H的表达来调控H3K9me3水平的。为进一步探究G2E3促进H3K9me3是否通过其催化的H3K14ub修饰, 我们将G2E3和酶活缺失突变体分别与组蛋白H3以及突变体H3K14R和H3K18R/K23R在293T细胞中过表达, 将过表达的组蛋白变性免疫沉淀, 检测H3K14ub和H3K9me3修饰。结果显示G2E3催化H3K14ub的同时促进H3K9me3修饰, 酶活缺失突变体丧失了此功能; 而H3K14R不能被G2E3催化单泛素化修饰, 其H3K9me3修饰水平亦没有变化; G2E3与野生型组蛋白H3共同过表达时, G2E3显著促进经H3K14ub修饰和未经H3K14ub修饰的组蛋白发生H3K9me3修饰(图2E), 表明H3K14ub同时存在顺式和反式两种方式促进H3K9me3修饰, 这更有利于H3K9me3在近着丝粒异染色质上快速扩散。这些实验结果表明G2E3以泛素连接酶活性依赖方式,通过其催化的H3K14ub特异性促进近着丝粒异染色质H3K9me3修饰。
我们发现G2E3敲低或者敲除导致近着丝粒异染色质H3K9me3剧烈下降的同时也导致近着丝粒异染色质区域SUV39H和HP1显著下调(图2F和图2G), 提示我们G2E3的缺失很可能影响SUV39H和HP1近着丝粒异染色质靶向定位从而调控H3K9me3修饰。为了探究SUV39H是否介导G2E3对H3K9me3的促进作用, 我们运用CRISPR-Cas9方法构建了SUV39H1敲除、SUV39H2敲除和SUV39H1/2双敲除的HeLa细胞系。WB和IF结果都显示SUV39H1敲除对H3K9me3影响微弱, SUV39H2敲除导致H3K9me3水平剧烈下降, SUV39H1/2双敲除后H3K9me3只剩极其微弱的残留, 且近着丝粒异染色质H3K9me3几乎完全丧失(图2H和图2I)。随后在这些敲除细胞系中过表达G2E3的实验结果显示SUV39H1敲除几乎不影响G2E3对H3K9me3的促进作用, SUV39H2敲除显著影响G2E3促进H3K9me3的能力, 而SUV39H1/2双敲除后G2E3丧失了对H3K9me3的促进作用(图2J)。这些结果表明SUV39H1/2蛋白共同介导了G2E3对近着丝粒异染色质H3K9me3修饰的促进作用。同时,我们也观察到SUV39H1/2的缺失轻微影响G2E3的异染色质定位, 但不影响G2E3对近着丝粒异染色质H3K14ub的催化作用。
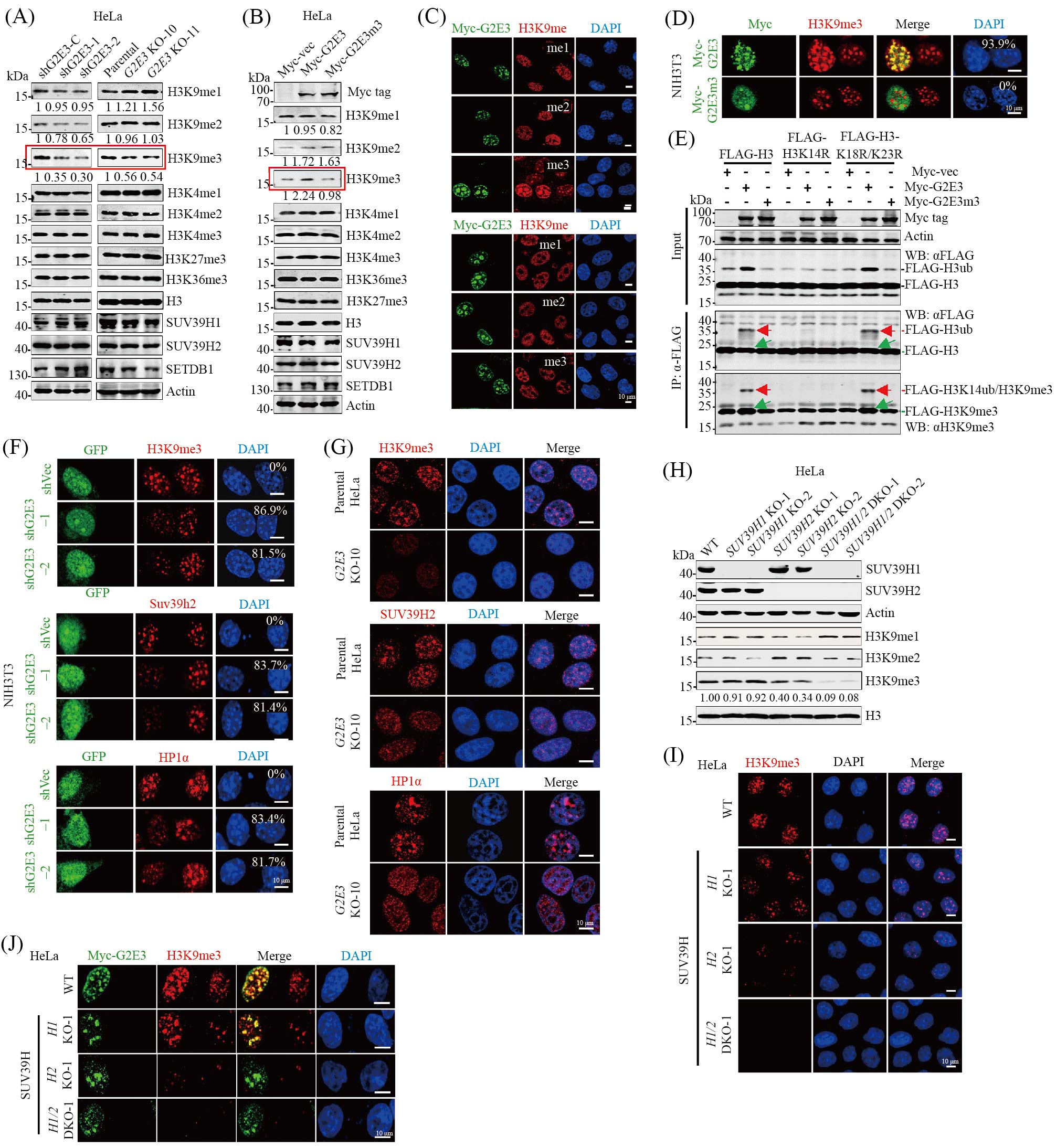
A: G2E3敲低或敲除特异性导致H3K9me3降低。B、C: HeLa细胞中过表达G2E3和酶活突变体, G2E3酶活依赖性特异性促进H3K9me3。D:NIH3T3细胞中过表达G2E3和酶活突变体, IF显示G2E3酶活依赖性促进H3K9me3。E: G2E3促进H3K9me3依赖于其催化的H3K14ub修饰。F:NIH3T3细胞中敲低G2E3导致内源H3K9me3剧烈下降, 同时SUV39H2和HP1α的异染色质定位水平剧烈降低。G: HeLa细胞中敲除G2E3导致内源H3K9me3剧烈下降, 同时SUV39H2和HP1α的异染色质定位水平剧烈降低。H、I: WB和IF检测SUV39H1/2敲除对H3K9甲基化的影响。J: IF显示SUV39H1/2双敲除后过表达G2E3不能促进H3K9me3。
A: knockdown or knockout of G2E3 impairs H3K9me3 specifically. B,C: ectopic expression of G2E3 but not G2E3m3 elevates H3K9me3 specifically in HeLa cells. D: ectopic expression of G2E3 but not G2E3m3 elevates H3K9me3 in NIH3T3 cells. E: G2E3 enhances H3K9me3 via H3K14ub modification. F: knockdown of G2E3 results in a dramatic decrease of endogenous H3K9me3, accompanied by a significant reduction of SUV39H2 and HP1α heterochromatin localization in NIH3T3 cells. G: knockout of G2E3 results in a dramatic decrease of endogenous H3K9me3, accompanied by a significant reduction of SUV39H2 and HP1α heterochromatin localization in HeLa cells. H,I: WB and IF analysis of the effect of SUV39H1/2 knockout on H3K9 methylation. J: IF showing that ectopically expressed G2E3 fails to enhance H3K9me3 after SUV39H1/2 double knockout.
图2 G2E3酶活依赖性促进SUV39H1/2介导的近着丝粒异染色质H3K9me3修饰(根据参考文献[29]修改)
Fig.2 G2E3 specifically promotes SUV39H-catalyzed heterochromatin H3K9me3 via its H3K14ub E3 ligase activity (modified from reference [29])
4 有丝分裂过程中G2E3通过其催化的H3K14ub调控SUV39H的近着丝粒异染色质靶向定位
G2E3包含三个PHD结构域和一个HECT结构域, 最初被鉴定为细胞有丝分裂G2/M期高表达的泛素连接酶[35-36]。由此, 我们对G2E3蛋白的细胞周期性变化进行了检测。由于缺乏特异性识别细胞内源G2E3蛋白的抗体, 我们通过CRISPR-Cas9基因敲入技术在内源G2E3的C-端敲入了3xHA标签, 构建了G2E3-3xHA HeLa细胞系。将此细胞系同步化到不同的时期, WB结果显示G2E3-3xHA蛋白在G2/M期高表达, H3K14ub也在G2/M期达到峰值(图3A)。在G2E3敲除的HeLa细胞中, G2/M期H3K14ub几乎完全丧失(图3B)。进一步IF结果显示在有丝分裂过程中G2E3-3xHA蛋白在G2/M期高表达, 并始终与染色体结合(图3C), 内源H3K14ub亦始终在染色体上, 并在有丝分裂后期达到峰值(图3D)。这些结果表明,G2E3在G2/M期高表达, 全程与有丝分裂染色体结合, 且催化了细胞内几乎所有的H3K14ub修饰, 尤其在细胞周期的G2/M期。
之前报道在酵母、秀丽隐杆线虫乃至哺乳动物细胞中, H3K9甲基转移酶都存在RNA依赖的异染色质定位机制[22-24,37-40]。鉴于G2E3在整个有丝分裂过程中持续结合染色体, 我们猜测RNA是否介导G2E3与染色体结合。我们将过表达Myc-G2E3的HeLa细胞同步化到M期, 0.5% Triton X-100通透后用RNaseA处理, 随后的免疫染色结果显示RNase A处理不影响H3K9me3, 但是过表达的Myc-G2E3绝大部分都从染色体上解离, 而没有RNase A处理的细胞, Myc-G2E3持续结合在染色体上(图3E)。我们进一步对HeLa细胞中过表达Myc-G2E3进行免疫沉淀实验并用定量PCR技术检测RNA的富集, 结果显示相较于18S rRNA、Actin mRNA和长链非编码RNA, 免疫沉淀的G2E3选择性富集多个卫星RNA(图3F)。由此,我们认为G2E3在近着丝粒异染色质富集并且在M期持续结合染色体很可能是通过直接或间接结合来源于近着丝粒异染色质重复序列的α-satellite RNA。
在细胞分裂周期中, 被DNA复制所破坏结构的近着丝粒异染色质需重新组装形成新的异染色质。先前研究表明SUV39H和HP1蛋白在有丝分裂期间会从染色质解离[41-43]。敲低或敲除G2E3, 都会导致SUV39H和HP1蛋白异染色质点状定位被剧烈削弱(图2F和图2G)。由此, 我们进而探究G2E3及其催化的H3K14ub是否促进有丝分裂后期SUV39H与HP1蛋白与近着丝粒异染色质的重新结合。与之前报道一致, 我们的结果显示SUV39H2和HP1α在有丝分裂中期不与浓缩的染色体结合, SUV39H2到有丝分裂后
期开始结合染色体, 此时H3K14ub水平最高; 而HP1α直到有丝分裂末期才结合到染色体上。当G2E3敲除后, SUV39H2和HP1α与浓缩染色体的结合能力严重受损, 并且这一现象持续到细胞间期(图3G)。这些结果表明, M期升高的H3K14ub在招募SUV39H参与近着丝粒异染色质重新建立过程中发挥关键作用, 并揭示了分子级联机制—在近着丝粒异染色质区域,G2E3催化的H3K14ub修饰招募SUV39H, 后者进而催化H3K9me3修饰以招募HP1蛋白。
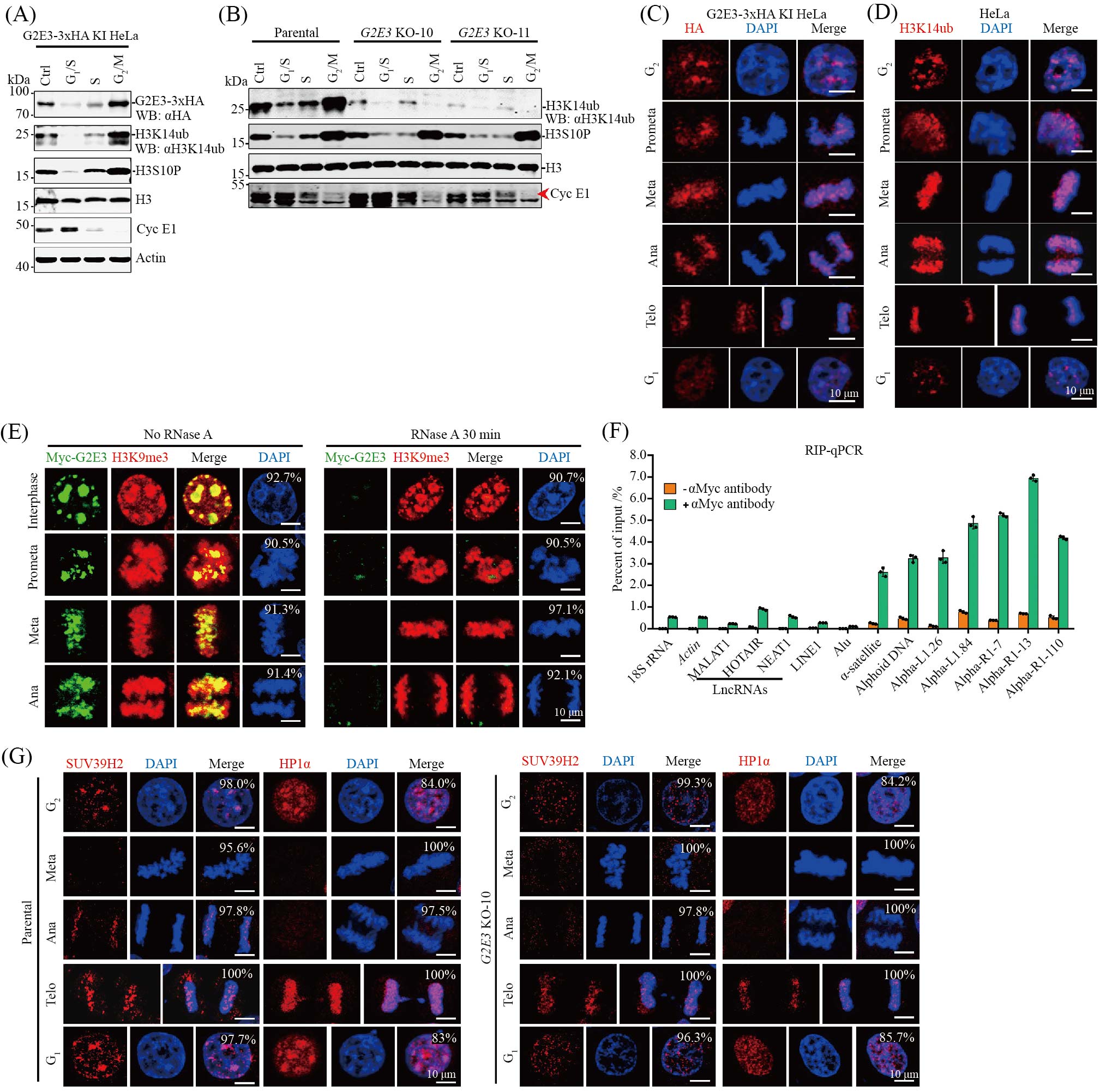
A: WB结果显示细胞内源G2E3和H3K14ub随细胞分裂周期变化, 在G2/M期高表达。B: G2/M期高丰度的H3K14ub由G2E3催化。C、D: 细胞内源G2E3和H3K14ub在细胞有丝分裂过程中始终结合在染色体上, 并在有丝分裂后期达到峰值。E: 有丝分裂过程中G2E3以RNA依赖的方式结合染色体。F: RIP-qPCR表明G2E3偏好结合近着丝粒和着丝粒satellite RNA(双侧多重配对t检验, n=3)。G: G2E3敲除导致有丝分裂过程中SUV39H2和HP1α靶向定位异染色能力剧烈下降。
A: WB shows endogenous G2E3 and H3K14ub are highly expressed in G2/M phase. B: G2E3 is responsible for the markedly elevated H3K14ub level in G2/M phase. C,D: endogenous G2E3 and H3K14ub associate with mitotic chromosomes along the mitosis process, and reach peak levels during metaphase. E: G2E3 associates with mitotic chromosomes in RNA-dependent manner. F: RIP-qPCR analysis showing preferential association of G2E3 with pericentromeric and centromeric a-satellite transcripts. Two sides multiple t tests-one per row paired-test using GraphPad Prism 8.0, n=3. G: G2E3 knockout violently affects SUV39H2 and HP1α targeting to mitotic chromosomes.
图3 有丝分裂过程中G2E3通过其催化的H3K14ub调控SUV39H的近着丝粒异染色质靶向定位(根据参考文献[29]修改)
Fig.3 G2E3 strongly catalyzes H3K14ub during G2/M phases to target SUV39H to pericentromeric heterochromatin (modified from reference [29])
5 SUV39H通过其Chromo结构域结合H3K14ub和H3K9me3而靶向定位近着丝粒异染色质
由于用免疫共沉淀实验检测不到G2E3和SUV39H1/2之间的相互作用(图4A), 并且G2E3对SUV39H1/2异染色质定位调控依赖H3K14ub, 因此猜测SUV39H1/2很可能通过直接结合H3K14ub而靶向定位近着丝粒异染色质。为验证这一猜想, 我们利用体外纯化GST-SUV39H1/2对过表达Myc-G2E3的293T细胞超声裂解液进行Pull-down实验, 结果显示具有K14单泛素化修饰的H3能够很好地被富集(图4B)。为了探究SUV39H1/2哪个结构域参与结合H3K14ub, 我们根据其功能结构域将SUV39H2分成了三个截短体, 发现只有N-端包含Chromo结构域的截短体能与G2E3共定位于近着丝粒异染色质(图4C)。之前的研究报道SUV39H/Clr4的Chromo结构域是H3K9me3/2的阅读器, 并在异染色质形成中发挥关键作用[44-45]。经AlphaFold结构模拟后进行分子对接, 结果显示SUV39H2的Chromo结构域可能可以同时结合H3K14ub和H3K9me3(图4D)。为了验证Chromo结构域是否能同时识别结合H3K14ub和H3K9me3, 及鉴定参与结合的关键氨基酸, 我们根据结构模拟结果对SUV39H2进行一系列点突变,并将其与Myc-G2E3在HeLa细胞中共转染, IF检测SUV39H2及其突变体与Myc-G2E3在近着丝粒异染色质的共定位情况。结果显示D54A突变和W78A突变都几乎丧失了与G2E3的共定位, W68A突变体与G2E3共定位轻微受损(图4D~图4E)。BiotinH3K9me3(1~21 aa)多肽Pull-down实验显示W68A突变和W78A突变影响SUV39H2与H3K9me3结合(图4F), 与之前报道Chromo结构域结合H3K9me3的关键氨基酸位点一致[46-48]。为了验证D54是否是结合H3K14ub的关键氨基酸, 我们体外纯化组蛋白H3和G2E3, 并进行体外泛素化反应, 得到带有K14ub修饰的组蛋白H3, 并检测其与体外纯化的GST-SUV39H2野生型和突变体的结合情况, 结果显示D54A突变和W78A突变都会剧烈影响SUV39H2与H3K14ub的结合(图4G)。这些结果表明SUV39H2的Chromo结构域具有识别并结合H3K14ub和H3K9me3的双重作用, D54特异参与结合H3K14ub, W68特异参与结合H3K9me3, 而这两种修饰的结合都需要W78参与。
W68虽然是结合H3K9me3的关键氨基酸, 但是W68A突变对SUV39H2与G2E3近着丝粒异染色质共定位的影响并不大, 而D54A突变几乎使共定位完全丧失(图4E), 提示SUV39H2近着丝粒异染色质定位主要是通过结合H3K14ub而不是H3K9me3。为了验证该推论, 我们以biotin-H3(1~21 aa)和biotin-H3K9me3(1~21 aa)多肽为底物, 体外纯化的G2E3为泛素连接酶做体外泛素化反应, 得到biotin-H3K14ub(1~21 aa)和biotin-H3K9me3/K14ub(1~21 aa)多肽。以此四种多肽做peptide-pull-down实验检测与GST-SUV39H2(1~105 aa) N-端Chromo结构域的结合能力, 结果显示, GST-SUV39H2(1~105 aa)结合H3K9me3多肽能力约是结合未修饰的H3多肽能力的6倍; 尽管只有约40%的多肽被单泛素化, 但GSTSUV39H2(1~105 aa)结合H3K14ub多肽能力增强到14倍。GST-SUV39H2(1~105 aa)结合H3K9me3/K14ub双修饰能力最强, 约为未修饰的H3多肽的19倍(图4H)。这些体外结合实验结果有力支持SUV39H1/2靶向定位近着丝粒异染色质主要依赖结合H3K14ub,并且H3K14ub和H3K9me3的协同作用能更好地保障SUV39H1/2的靶向定位。同时我们也观察到, 在SUV39H2敲除细胞中过表达SUV39H2野生型和突变体时, D54A、W68A和W78A突变体催化H3K9me3能力与野生型相比下降(图4I), 表明结合H3K14ub或者(和)H3K9me3会增强SUV39H1/2甲基转移酶活性。
与我们结果一致, 最新的研究报道从结构上解析酵母H3K9甲基转移酶Clr4存在两个泛素结合位点(UBS), UBS1在其SET结构域, 能够结合H3K14ub并顺式催化同一个H3蛋白的K9发生K9me2/3修饰; USB2在Chromo结构域, Chromo结构域同时结合H3K14ub和H3K9me2/3, SET结构域反式催化临近的H3蛋白发生K9me2/3修饰[49], 这两种方式并存保障了H3K9甲基化在异染色质区域扩散的效率。
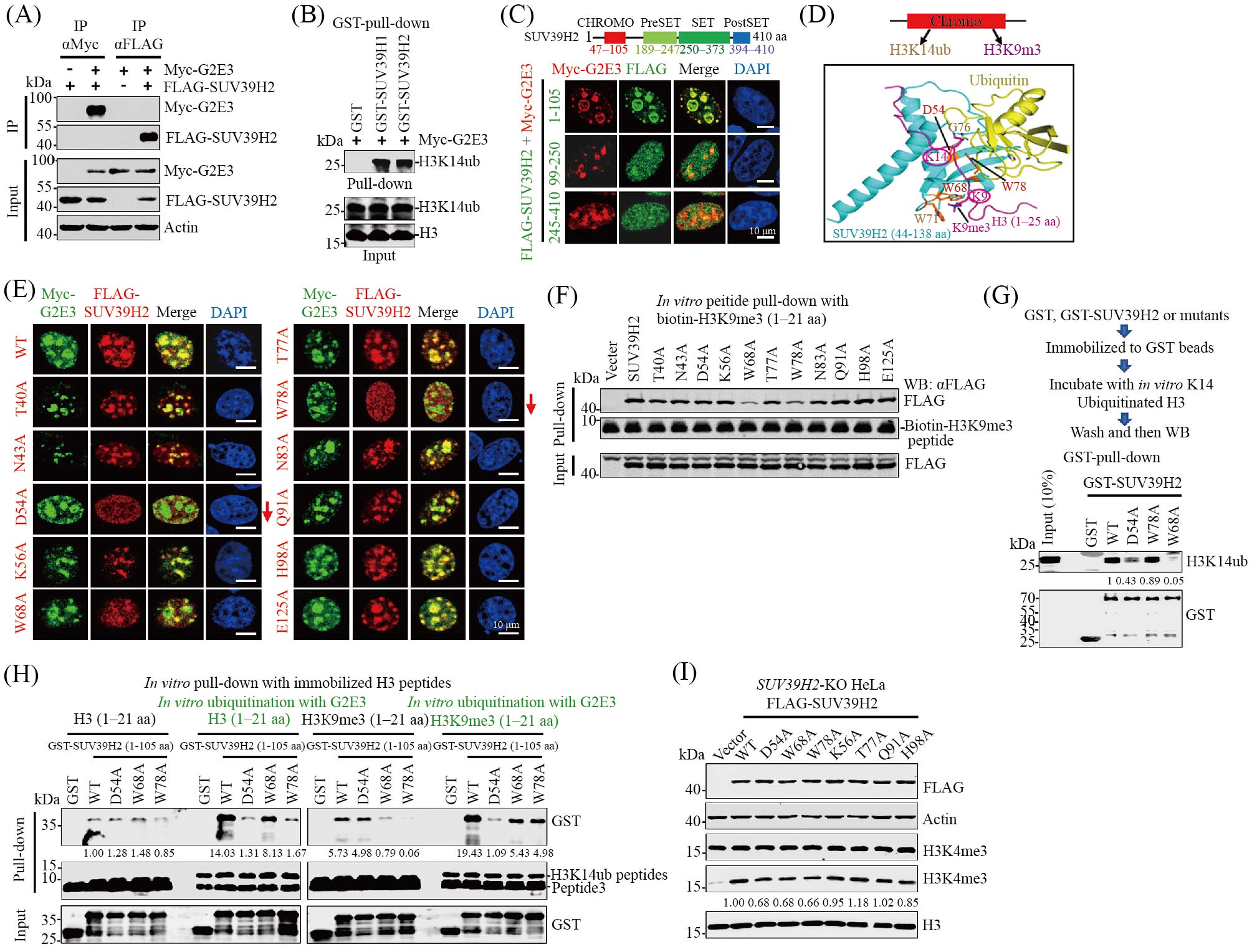
A: IP-WB结果显示过表达的G2E3与SUV39H2没有相互作用。B: GST-pull-down结果显示体外纯化的GST-SUV39H1/2都能与K14单泛素化修饰的H3结合。C: SUV39H2的N-端1—105 aa对于SUV39H2与G2E3共定位是必要的。D: 分子对接提示SUV39H2的Chromo结构域同时结合H3K14ub和H3K9me3。E: IF检测SUV39H2突变体的异染色质结合情况。F: histone tail pull-down检测SUV39H2突变体与H3K9me3的结合情况。G: GST-pull-down结果显示D54A和W78A突变影响SUV39H2与H3K14ub的结合。H: histone tail pull-down检测SUV39H2的Chromo结构域和突变体与H3、H3K14ub、H3K9me3及H3K9me3/K14ub peptide的结合情况。I: 在SUV39H2 KO HeLa细胞中过表达SUV39H2和突变体, 结果显示D54A、W68A和W78A影响SUV39H2催化H3K9me3的活性。
A: IP-WB indicates no interaction between ectopically expressed G2E3 and SUV39H2. B: GST-pull-down showing that both in vitro purified GSTSUV39H1/2 can bind to K14 monoubiquitinated H3. C: the N-terminal 1—105 aa of SUV39H2 is essential for SUV39H2 colocalization with G2E3. D: molecular docking suggests the Chromo domain of SUV39H2 binds H3K14ub and H3K9me3 simultaneously. E: IF analysis of SUV39H2 mutants binding to heterochromatin. F: histone tail pull-down assay demonstrating the effect of SUV39H2 mutants binding to H3K9me3. G: GST-pull-down demonstrates that D54A and W78A mutants are impaired in binding H3K14ub. H: histone tail pull-down assay evaluates the relative binding affinity of SUV39H2 chromodomain and mutants for H3, H3K14ub, H3K9me3, and H3K9me3/H3K14ub peptides. I: ectopic expression of SUV39H2 and its mutants in SUV39H2 KO HeLa cells revealed that D54A, W68A, and W78A mutants impair catalytic activity for H3K9me3.
图4 SUV39H通过其Chromo结构域同时结合H3K14ub和H3K9me3而靶向定位近着丝粒异染色质(根据参考文献[29]修改)
Fig.4 The SUV39H chromodomain is a dual functional reader of H3K14ub and H3K9me3, and critical for SUV39H targeting to pericentromeric heterochromatin (modified from reference [29])
6 全基因组分析显示近着丝粒异染色质区域的H3K9me3与H3K14ub高度关联
为了阐明G2E3催化的H3K14ub在全基因组范围与H3K9me3的关联性, 我们对亲代细胞和G2E3 KO HeLa细胞进行了ChIP-seq实验。分析显示在亲代对照细胞中鉴定到6 286个H3K14ub峰, 其中5 564个同时存在H3K9me3峰, 且几乎没有共存的H3K4me3峰。当G2E3敲除后原有的H3K14ub和H3K9me3的峰数目和强度都急剧下降(图5A)。进一步分析显示, 重叠的H3K14ub与H3K9me3峰在近着丝粒卫星序列及着丝粒α-卫星重复序列区域高度富集, 且当G2E3敲除后, H3K14ub和H3K9me3信号在上述区域均剧烈降低(图5B)。代表性的基因组截图清晰显示H3K14ub和H3K9me3在近着丝粒和着丝粒区域富集, 而G2E3敲除后这两种修饰均显著减少(图5D)。值的注意的是H3K14ub在LINE1、Alu和ERVK等重复序列中并没有富集, 且G2E3敲除并不会导致这些区域H3K9me3水平的下降, 反而略微上升(图5C)。通过ChIP-qPCR分析, 我们证实H3K9me3在spc、alphoid和alpha-R1-7等近着丝粒和着丝粒重复序列中高度富集, G2E3敲除导致H3K9me3水平在这些序列上显著降低, 以及在LINE1、Alu和ERVK序列上轻微升高(图5E)。同时G2E3的缺失也削弱了SUV39H2在这些近着丝粒和着丝粒重复序列上的结合, 却促进了SUV39H2在LINE1、Alu和ERVK等序列的结合(图5F)。qPCR结果显示G2E3敲除导致近着丝粒和着丝粒重复序列的转录水平上调(图
5G)。综上所述, H3K14ub和H3K9me3在近着丝粒和着丝粒区域富集, G2E3敲除导致这些区域H3K14ub缺失, SUV39H的靶向定位受损, 进而导致H3K9me3剧烈下调, 异染色质结构的破坏, 原本转录沉默的近着丝粒和着丝粒重复序列的转录水平升高。
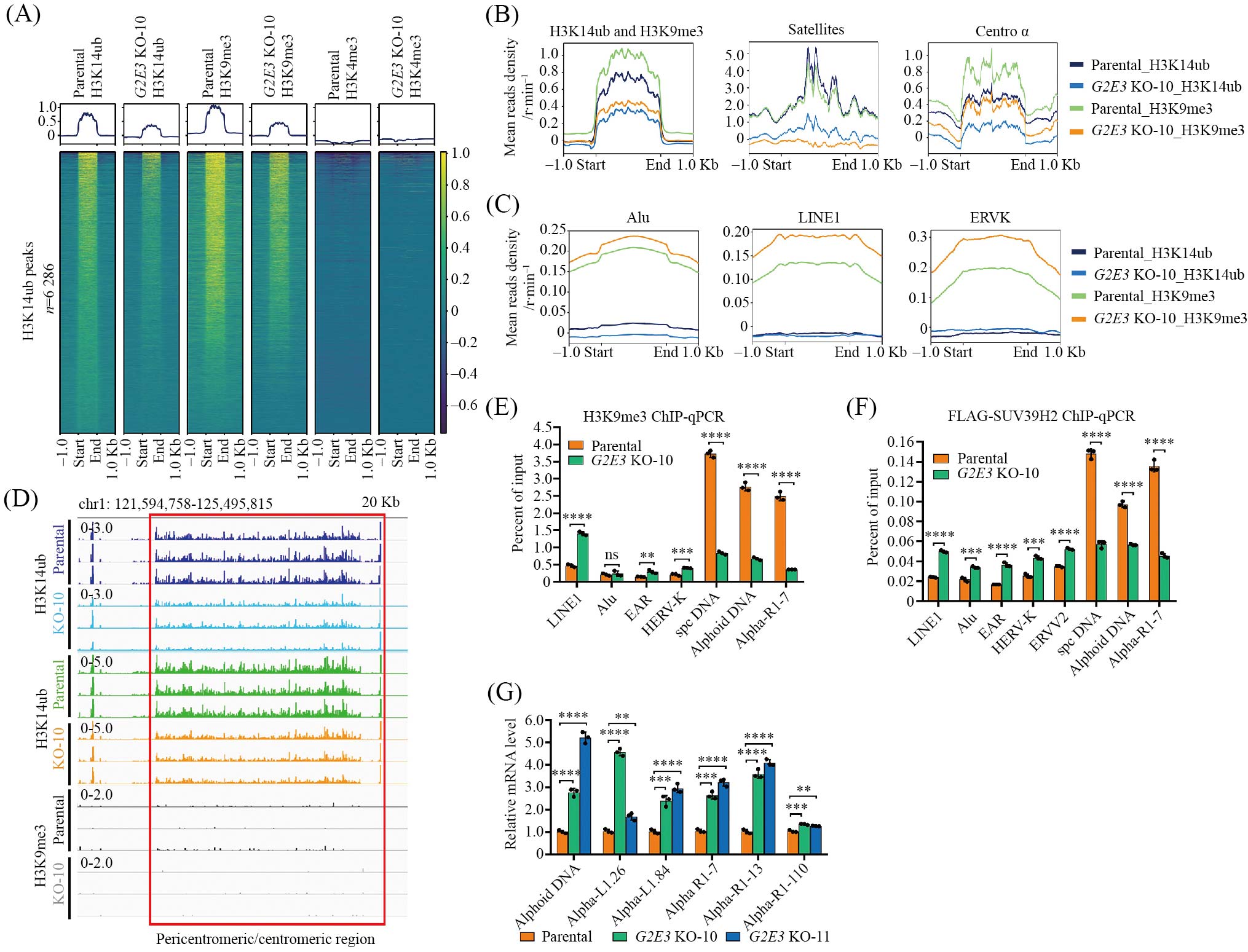
A: ChIP-seq均值热图展示亲代和G2E3 KO HeLa细胞的H3K14ub峰, 以及与之对应的H3K9me3峰和H3K4me3峰(n=3)。B: H3K14ub峰富集在satellite和Centro α-satellite序列, G2E3敲除后整体以及satellite和Centro α-satellite序列的H3K14ub和H3K9me3都剧烈下降。C: Alu、LINE1和ERVK序列没有H3K14ub修饰, G2E3敲除导致这些序列的H3K9me3轻微升高。D: Track图展示H3K14ub和H3K9me3在1号染色体近着丝粒和着丝粒区域高度富集, G2E3敲除导致H3K14ub和H3K9me3剧烈下降。E: ChIP-qPCR结果显示G2E3敲除后satellite序列H3K9me3修饰降低,LINE1、Alu和ERVK序列H3K9me3修饰轻微升高。 F: ChIP-qPCR结果显示G2E3敲除后SUV39H2在satellite序列上结合减弱, 在LINE1、Alu和ERVK序列上结合增强。 G: qPCR结果显示G2E3敲除后近着丝粒异染色质satellite和着丝粒重复序列的转录水平升高。统计分析均采用双侧多重配对t检验, x_±s, n=3, **P<0.01; ***P<0.001; ****P<0.000 1; ns: 无统计学意义。
A: average heatmap displays H3K14ub peaks in parental and G2E3 KO HeLa cells, and corresponding H3K9me3 and H3K4me3 peaks (n=3). B: H3K14ub peaks are enriched in satellite and Centro α-satellite sequences. G2E3 knockout results in dramatic decrease of H3K14ub and H3K9me3 in all H3K14ub peaks, especially in satellite and Centro α-satellite sequences. C: G2E3 KO results in H3K9me3 levels slightly increased in Alu, LINE1, and ERVK sequences which lack of H3K14ub. D: track plot shows high enrichment of H3K14ub and H3K9me3 in the pericentromeric and centromeric regions of chromosome 1. G2E3 knockout results in dramatic decrease in H3K14ub and H3K9me3. E: ChIP-qPCR indicates reduced H3K9me3 modification in satellite sequences and slight increases in LINE1, Alu, and ERVK sequences following G2E3 knockout. F: ChIP-qPCR indicates weakened SUV39H2 binding at satellite sequences and enhanced binding at LINE1, Alu, and ERVK sequences after G2E3 knockout. G: qPCR shows elevated transcription levels of pericentromeric satellite repeat and centromere repeat transcripts in two G2E3 KO HeLa cell lines. All statistical analysis was performed two sides multiple t tests-one per row using GraphPad Prism 8.0, x_±s, n=3, **P<0.01; ***P<0.001; ****P<0.000 1; ns: no statistical significance.
图5 H3K14ub在近着丝粒异染色质高度富集且与H3K9me3高度关联(根据参考文献[29]修改)
Fig.5 H3K14ub is highly enriched at and required for H3K9me3 in pericentromeric heterochromatin (modified from reference [29])
7 G2E3调控常染色质的区室化和功能
我们意外发现, G2E3敲除后H3K9me3峰数目和强度在近着丝粒和着丝粒区域显著降低, 但H3K-9me3峰的总数却显著上调, 从亲代细胞中的17 114增加到G2E3敲除细胞中的43 711。这些H3K9me3峰经分析聚类可为三组, 第一组在亲代细胞中H3K-9me3峰很微弱甚至没有, G2E3敲除导致这些区域13 217个峰增强或新增, 这些区域没有H3K14ub修饰; 第二组在亲代细胞中有很强H3K9me3峰, G2E3敲除导致H3K9me3峰剧烈下降, 这些峰同时也是H3K14ub富集的区域; 第三类在亲代中存在较弱的H3K9me3峰, G2E3敲除导致其微弱增强或者不变,这些区域很少存在H3K14ub修饰(图6A)。进一步分析显示第二组聚集在近着丝粒和着丝粒区域, G2E3敲除导致H3K14ub下降的同时也导致H3K9me3显著下降; 第一组和第三组主要聚集在常染色质区域, 这些区域几乎没有H3K14ub修饰, G2E3敲除反而导致其H3K9me3广泛上调(图6B~图6C)。
常染色质区域H3K9me3的广泛上调促使我们检测G2E3敲除对基因表达的影响。为了确保数据的重复性和可靠性, 我们将亲代对照细胞和两株G2E3敲除细胞系, G2E3 KO-10和G2E3 KO-11, 同时进行RNA-seq。结果检测到15 381个测序读段(reads)>10的共有基因, 当以基因转录1.5倍变化量, P<0.05为阈值时, 两株G2E3敲除细胞系共同下调基因有5 123个, 共同上调基因只有603个(图6D), 并且共同下调基因中有56%在基因体或者基因上下游20 Kb内存在H3K9me3修饰上调。代表性的基因组区域展示了G2E3敲除导致常染色质H3K9me3上升, 基因转录抑制(图6E)。通过qPCR我们进一步证实G2E3敲除导致基因转录抑制(图6F)。ChIP-qPCR结果显示这些转录受抑制的基因区域内SUV39H2结合增强(图6G), H3K9me3丰度升高(图6H)。这些数据表明G2E3敲除导致原本靶向近着丝粒异染色质的SUV39H重新分布到常染色质, 催化广泛的H3K9me3修饰, 导致基因转录广谱抑制。这些结果也表明G2E3通过将SUV39H和H3K9me3束缚在近着丝粒异染色质区域不仅对异染色质形成和稳态遗传极为重要, 同时对常染色质的正常区室化和功能也是必要的。与我们结果一致, 最新的研究报道在小鼠细胞中Suv39h催化的H3K9me3对常染色质结构的建立以及基因转录的维持至关重要[50]。
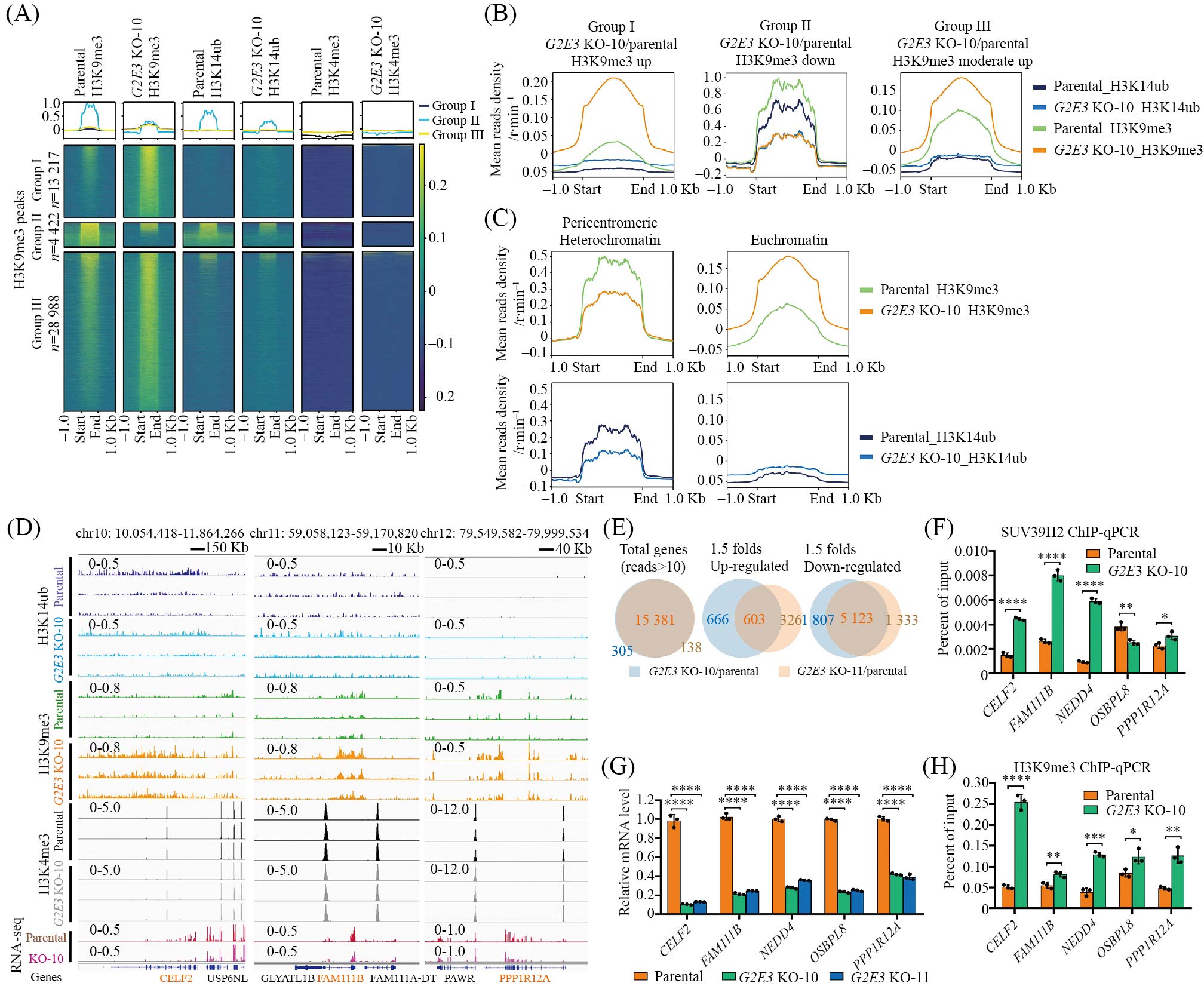
A: ChIP-seq均值热图按照H3K9me3变化情况聚类成三组展示亲代和G2E3 KO HeLa细胞的H3K9me3峰, 以及与之对应的H3K14ub峰和H3K4me3峰(n=3)。B: 峰密度图分别展示三组峰区域内G2E3敲除前后H3K9me3和H3K14ub的变化情况。C: 上部分显示G2E3敲除导致近着丝粒异染色质H3K9me3显著降低, 常染色质H3K9me3升高。下部分显示H3K14ub在近着丝粒异染色质而不是常染色质富集。D: Track图显示G2E3敲除后常染色质H3K9me3上升, 基因转录水平下降。E: 两株G2E3 KO HeLa细胞的RNA-seq结果显示G2E3敲除导致广泛的基因转录抑制。F: ChIP-qPCR显示G2E3敲除后SUV39H2在转录下调基因上结合增加。G: qPCR结果显示G2E3敲除后五个代表性基因转录水平下降。 H: ChIP-qPCR显示G2E3敲除后转录下调基因区域的H3K9me3上调。统计分析均采用双侧多重配对t检验, x_±s, n=3, *P<0.05; **P<0.01; ***P<0.001; ****P<0.000 1。
A: average heatmaps cluster H3K9me3 peaks from parental and G2E3 KO HeLa cells into three groups based on H3K9me3 changes, alongside corresponding H3K14ub and H3K4me3 peaks (n=3). B: peak density profiles of H3K9me3 and H3K14ub in group I, group II, and group III peaks. C: top panels show that G2E3 knockout causes a significant loss of H3K9me3 in pericentromeric heterochromatin and a substantial gain of H3K9me3 in euchromatin. Bottom panels show H3K14ub is enriched in pericentromeric heterochromatin but absent in euchromatin. D: track plot showing that H3K9me3 increases in euchromatin and transcription decreases after G2E3 knockout. E: RNA-seq of two G2E3 KO HeLa cell lines reveal extensive transcriptional repression following G2E3 knockout. F: ChIP-qPCR indicates increased SUV39H2 binding to transcriptionally downregulated genes after G2E3 knockout. G: qPCR indicates that the transcription levels of five representative genes decreased following G2E3 knockout. H: ChIP-qPCR reveals upregulation of H3K9me3 in regions of transcriptionally downregulated genes after G2E3 knockout. All statistical analysis was performed two sides multiple t tests-one per row using GraphPad Prism 8.0, x_±s, n=3, *P<0.05; **P<0.01; ***P<0.001; ****P<0.000 1.
图6 G2E3调控常染色质正常区室化和基因转录(根据参考文献[29]修改)
Fig.6 G2E3 is required for appropriate euchromatin compartmentation and transcriptional regulation (modified from reference [29])
8 总结与展望
虽然很早就知道H3K9me3修饰是异染色质正确形成、维持和稳态遗传的关键, 但其在细胞分裂过程中如何被稳定“继承”一直被认为是通过简单的自模板“读写”能力。我们的研究发现了哺乳动物细胞中催化H3K14ub的关键泛素连接酶G2E3, 首次在哺乳动物中揭示了H3K14ub驱动的H3K9me3修饰的异染色质维持和稳态遗传机制。尽管酵母和哺乳动物使用不同的泛素连接酶, 但它们都通过“H3K14ub→H3K9me3”这一共同路径来实现近着丝粒异染色质的稳态遗传, 同时影响常染色质的正常区室化和功能, 表明该机制在进化上高度保守, 是生命体的“基础设计”。由此, 我们提出一个着丝粒异染色质稳态维持的统一假说: 无论在裂殖酵母还是哺乳动物细胞中, S期均会出现近着丝粒重复序列转录水平的升高, 这可能源于异染色质结构的暂时性破坏; 在哺乳动物细胞中转录自近着丝粒相关序列的RNA分子与核小体结合, 介导G2E3结合近着丝粒异染色质, 并在亲本及新组装的核小体组蛋白H3上催化H3K14ub修饰; 在G2/M期后期/末期阶段H3K14ub单独或者协同H3K9me3通过相互作用招募SUV39H1/2靶向定位于近着丝粒异染色质, 催化H3K9me3修饰; 随后HP1蛋白通过结合H3K9me3及与SUV39H1/2和(或) RNA的相互作用被招募, 进一步巩固近着丝粒异染色质; 在异染色质形成过程中SUV39H1/2被锁定并限制在近着丝粒异染色质, 防止其在常染色质的异常结合, 从而维持适当的染色质区室化与基因表达。而在裂殖酵母中, CLRC复合体也通过H3K14ub促进H3K9甲基化来促进异染色质的形成与稳态维持。
鉴于最新研究进展, 后续有必要探究G2E3与ZNF512/512B是否在近着丝粒异染色质形成过程中协同作用[51]。哺乳动物成熟的精子和卵子带有不同的表观修饰谱式和不同的染色质结构状态, 受精后,精子和卵子都会擦除各自的表观修饰谱式, 从而重新建立共有的表观修饰谱式[52-54]。此过程伴随着染色质结构的开放和重新建立, 我们后续将继续探索G2E3及其催化的H3K14ub在早期胚胎发育过程中对异染色质建立和成熟的调控功能与作用机制。
参考文献 (References)
[1] ALLSHIRE R C, MADHANI H D. Ten principles of heterochromatin formation and function [J]. Nat Rev Mol Cell Biol, 2018, 19(4): 229-44.
[2] SAKSOUK N, SIMBOECK E, DEJARDIN J. Constitutive heterochromatin formation and transcription in mammals [J]. Epigenetics Chromatin, 2015, 8: 3.
[3] GHOSH R P, MEYER B J. Spatial organization of chromatin: emergence of chromatin structure during development [J]. Annu Rev Cell Dev Biol, 2021, 37: 199-232.
[4] JANSSEN A, COLMENARES S U, KARPEN G H. Heterochromatin: guardian of the genome [J]. Annu Rev Cell Dev Biol, 2018, 34: 265-88.
[5] PENAGOS-PUIG A, FURLAN-MAGARIL M. Heterochromatin as an important driver of genome organization [J]. Front Cell Dev Biol, 2020, 8: 579137.
[6] CHEN P, LI W, LI G H. Structures and functions of chromatin fibers [J]. Annu Rev Biophys, 2021, 50: 95-116.
[7] LEE S K, WANG W D. Roles of topoisomerases in heterochromatin, aging, and diseases [J]. Genes, 2019, 10(11): 884.
[8] FISHER R M A, TORRENTE M P. Histone post-translational modification and heterochromatin alterations in neurodegeneration: revealing novel disease pathways and potential therapeutics [J]. Front Mol Neurosci, 2024, 17: 1456052.
[9] WU Z M, QU J, LIU G H. Roles of chromatin and genome instability in cellular senescence and their relevance to ageing and related diseases [J]. Nat Rev Mol Cell Bio, 2024, 25(12): 979-1000.
[10] YU R, WANG X, MOAZED D. Epigenetic inheritance mediated by coupling of RNAi and histone H3K9 methylation [J]. Nature, 2018, 558(7711): 615-9.
[11] MONTAVON T, SHUKEIR N, ERIKSON G, et al. Complete loss of H3K9 methylation dissolves mouse heterochromatin organization [J]. Nat Commun, 2021, 12(1): 4359.
[12] NAKAYAMA J, RICE J C, STRAHL B D, et al. Role of histone H3 lysine 9 methylation in epigenetic control of heterochromatin assembly [J]. Science, 2001, 292(5514): 110-3.
[13] PETERS A H, O’CARROLL D, SCHERTHAN H, et al. Loss of the Suv39h histone methyltransferases impairs mammalian heterochromatin and genome stability [J]. Cell, 2001, 107(3): 323-37.
[14] BANNISTER A J, ZEGERMAN P, PARTRIDGE J F, et al. Selective recognition of methylated lysine 9 on histone H3 by the HP1 chromo domain [J]. Nature, 2001, 410(6824): 120-4.
[15] LACHNER M, O’CARROLL D, REA S, et al. Methylation of histone H3 lysine 9 creates a binding site for HP1 proteins [J]. Nature, 2001, 410(6824): 116-20.
[16] LOMBERK G, WALLRATH L, URRUTIA R. The heterochromatin protein 1 family [J]. Genome Biol, 2006, 7(7): 228.
[17] ZENK F, ZHAN Y, KOS P, et al. HP1 drives de novo 3D genome reorganization in early Drosophila embryos [J]. Nature, 2021, 593(7858): 289-93.
[18] GREWAL S I S. The molecular basis of heterochromatin assembly and epigenetic inheritance [J]. Mol Cell, 2023, 83(11): 1767-85.
[19] HALL I M, SHANKARANARAYANA G D, NOMA K I, et al. Establishment and maintenance of a heterochromatin domain [J]. Science, 2002, 297(5590): 2232-7.
[20] REINHART B J, BARTEL D P. Small RNAs correspond to centromere heterochromatic repeats [J]. Science, 2002, 297(5588): 1831.
[21] VOLPE T A, KIDNER C, HALL I M, et al. Regulation of heterochromatic silencing and histone H3 lysine-9 methylation by RNAi [J]. Science, 2002, 297(5588): 1833-7.
[22] CAMACHO O V, GALAN C, SWIST-ROSOWSKA K, et al. Major satellite repeat RNA stabilize heterochromatin retention of Suv39h enzymes by RNA-nucleosome association and RNA:DNA hybrid formation [J]. eLife, 2017, 6: e25293.
[23] JOHNSON W L, YEWDELL W T, BELL J C, et al. RNA-dependent stabilization of SUV39H1 at constitutive heterochromatin [J]. eLife, 2017, 6: e25299.
[24] SHIRAI A, KAWAGUCHI T, SHIMOJO H, et al. Impact of nucleic acid and methylated H3K9 binding activities of Suv39h1 on its heterochromatin assembly [J]. eLife, 2017, 6: e25317.
[25] HONG E J, VILLEN J, GERACE E L, et al. A cullin E3 ubiquitin ligase complex associates with Rik1 and the Clr4 histone H3-K9 methyltransferase and is required for RNAi-mediated heterochromatin formation [J]. RNA Biol, 2005, 2(3): 106-11.
[26] HORN P J, BASTIE J N, PETERSON C L. A Rik1-associated, cullin-dependent E3 ubiquitin ligase is essential for heterochromatin formation [J]. Genes Dev, 2005, 19(14): 1705-14.
[27] JIA S, KOBAYASHI R, GREWAL S I. Ubiquitin ligase component Cul4 associates with Clr4 histone methyltransferase to assemble heterochromatin [J]. Nat Cell Biol, 2005, 7(10): 1007-13.
[28] OYA E, NAKAGAWA R, YOSHIMURA Y, et al. H3K14 ubiquitylation promotes H3K9 methylation for heterochromatin assembly [J]. Embo Rep, 2019, 20(10): e48111.
[29] HUANG Y Y, SUN Y M, QI H Y, et al. A conserved H3K14ubdriven H3K9me3 for chromatin compartmentalization [J]. Nature, 2025, 647(8090): 786-97.
[30] KIM C R, NODA T, KIM H, et al. PHF7 modulates BRDT stability and histone-to-protamine exchange during spermiogenesis [J]. Cell Rep, 2020, 32(4): 107950.
[31] BLACKLEDGE N P, FARCAS A M, KONDO T, et al. Variant PRC1 complex-dependent H2A ubiquitylation drives PRC2 recruitment and polycomb domain formation [J]. Cell, 2014, 157(6): 1445-59.
[32] COOPER S, DIENSTBIER M, HASSAN R, et al. Targeting polycomb to pericentric heterochromatin in embryonic stem cells reveals a role for H2AK119u1 in PRC2 recruitment [J]. Cell Rep, 2014, 7(5): 1456-70.
[33] KIM J, GUERMAH M, MCGINTY R K, et al. RAD6-mediated transcription-coupled H2B ubiquitylation directly stimulates H3K4 methylation in human cells [J]. Cell, 2009, 137(3): 459-71.
[34] WORDEN E J, HOFFMANN N A, HICKS C W, et al. Mechanism of cross-talk between H2B ubiquitination and H3 methylation by Dot1L [J]. Cell, 2019, 176(6): 1490-501.
[35] CRAWFORD D F, PIWNICA-WORMS H. The G(2) DNA damage checkpoint delays expression of genes encoding mitotic regulators [J]. J Biol Chem, 2001, 276(40): 37166-77.
[36] BROOKS W S, HELTON E S, BANERJEE S, et al. G2E3 is a dual function ubiquitin ligase required for early embryonic development [J]. J Biol Chem, 2008, 283(32): 22304-15.
[37] MAISON C, BAILLY D, PETERS A H F M, et al. Higher-order structure in pericentric heterochromatin involves a distinct pattern of histone modification and an RNA component [J]. Nat Genet, 2002, 30(3): 329-34.
[38] MOTAMEDI M R, VERDEL A, COLMENARES S U, et al. Two RNAi complexes, RITS and RDRC, physically interact and localize to noncoding centromeric RNAs [J]. Cell, 2004, 119(6): 789-802.
[39] BÜHLER M, VERDEL A, MOAZED D. Tethering RITS to a nascent transcript initiates RNAi- and heterochromatin-dependent gene silencing [J]. Cell, 2006, 125(5): 873-86.
[40] LI X, FU X D. Chromatin-associated RNAs as facilitators of functional genomic interactions [J]. Nat Rev Genet, 2019, 20(9): 503-19.
[41] AAGAARD L, SCHMID M, WARBURTON P, et al. Mitotic phosphorylation of SUV39H1, a novel component of active centromeres, coincides with transient accumulation at mammalian centromeres [J]. J Cell Sci, 2000, 113(5): 817-29.
[42] FISCHLE W, TSENG B S, DORMANN H L, et al. Regulation of HP1-chromatin binding by histone H3 methylation and phosphorylation [J]. Nature, 2005, 438(7071): 1116-22.
[43] HIROTA T, LIPP J J, TOH B H, et al. Histone H3 serine 10 phosphorylation by Aurora B causes HP1 dissociation from heterochromatin [J]. Nature, 2005, 438(7071): 1176-80.
[44] ZHANG K, MOSCH K, FISCHLE W, et al. Roles of the Clr4 methyltransferase complex in nucleation, spreading and maintenance of heterochromatin [J]. Nat Struct Mol Biol, 2008, 15(4): 381-8.
[45] AL-SADY B, MADHANI H D, NARLIKAR G J. Division of labor between the chromodomains of HP1 and Suv39 methylase enables coordination of heterochromatin spread [J]. Molecular Cell, 2013, 51(1): 80-91.
[46] JACOBS S A, KHORASANIZADEH S. Structure of HP1 chromodomain bound to a lysine 9-methylated histone H3 tail [J]. Science, 2002, 295(5562): 2080-3.
[47] NIELSEN P R, NIETLISPACH D, MOTT H R, et al. Structure of the HP1 chromodomain bound to histone H3 methylated at lysine 9 [J]. Nature, 2002, 416(6876): 103-7.
[48] WANG T, XU C, LIU Y L, et al. Crystal structure of the human SUV39H1 chromodomain and its recognition of histone H3K-9me2/3 [J]. PLoS One, 2012, 7(12): e52977.
[49] PSENAKOVA K, PARHAD S S, PAULO J A O X, et al. Catalytic pocket of Clr4 (Suv39h) methyltransferase serves as a substrate receptor for Cullin 4-dependent histone H3 ubiquitination [J]. bioRxiv, 2025, doi: 10.1101/2025.08.28.672867.
[50] KEENAN C R, COUGHLAN H D, IANNARELLA N, et al. Suv39h-catalyzed H3K9me3 is critical for euchromatic genome organization and the maintenance of gene transcription [J]. Genome Res, 2024, 34(4): 556-71.
[51] MA R Z, ZHANG Y, ZHANG J, et al. Targeting pericentric nonconsecutive motifs for heterochromatin initiation [J]. Nature, 2024, 631(8021): 678-85.
[52] DU Z H, ZHANG K, XIE W. Epigenetic reprogramming in early animal development [J]. Csh Perspect Biol, 2022, 14(6): a039677.
[53] WILKINSON A L, ZORZAN I, RUGG-GUNN P J. Epigenetic regulation of early human embryo development [J]. Cell Stem Cell, 2023, 30(12): 1569-84.
[54] ZOU Z N, WANG Q Y, WU X, et al. Kick-starting the zygotic genome: licensors, specifiers, and beyond [J]. Embo Rep, 2024, 25(10): 4113-30.




 中文版
中文版 英文版
英文版